
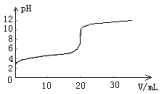
 常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )| A. | 在反应过程中,c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | pH=5时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | pH=7时,消耗NaOH溶液的体积肯定小于20.00mL | |
| D. | pH>7时,消耗NaOH溶液的体积肯定大于20.00mL |
分析 A.反应后的溶液一定满足电荷守恒,根据电荷守恒分析;
B.pH=5时,溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒判断;
C.如果消耗NaOH溶液的体积20.00mL,两者恰好完全反应生成醋酸钠,溶液呈碱性,若为中性,则加入的氢氧化钠溶液体积小于20.00mL;
D.如果消耗NaOH溶液的体积20.00mL,两者恰好完全反应生成醋酸钠,溶液呈碱性,若为中性,则加入的氢氧化钠溶液体积小于20.00mL,若为碱性,则加入的氢氧化钠溶液体积等于或是大于20.00mL.
解答 解:A.在反应过程中,一定满足电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故A正确;
B.pH=5的溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒可知:c(CH3COO-)>c(Na+),则溶液中离子浓度的大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故B正确;
C.如果消耗NaOH溶液的体积20.00mL,两者恰好完全反应生成醋酸钠,溶液呈碱性,若为中性,则加入的氢氧化钠溶液体积小于20.00mL,故C正确;
D.如果消耗NaOH溶液的体积20.00mL,两者恰好完全反应生成醋酸钠,溶液水解呈碱性,若使溶液呈中性,则消耗NaOH溶液的体积小于20.00mL,pH>7时,消耗NaOH溶液的体积大于或是等于20.00mL,故D错误;
故选D.
点评 本题考查酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确各点对应溶质组成为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理在判断离子浓度大小中的应用,试题培养了学生的分析、理解能力及灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:实验题
 .
. .
.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 | B. | N2 | C. | O2 | D. | CO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢化物的稳定:B>C | |
| B. | 简单离子的半径:D>C | |
| C. | 最高氧化物对应的水化物的酸性:B>D | |
| D. | BC2、D2C3中化学键类型相冋 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定含有Fe3+和Fe2+,肯定没有Cu2+ | |
| B. | 肯定含有Fe3+,肯定没有Cu2+,可能含Fe2+ | |
| C. | 肯定含有Cu2+,肯定没有Fe3+,可能含有Fe2+ | |
| D. | 肯定含有Fe2+,肯定没有Fe3+,可能含有 Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X是第IA元素,Y的最高正价是+3价 | |
| B. | Z是周期表中非金属性最强的元素 | |
| C. | 化合物XZ中含有离子键 | |
| D. | Y的单质与X、Z的最高价氧化物的水化物也都能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减少CO2的排放,可以减少酸雨的产生 | |
| B. | 减少SO2的排放,可以从根本上消除雾霾 | |
| C. | 用电镀厂的废水直接灌溉农田,可提高水的利用率 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com