
【题目】在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)![]() 2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
A.生成B的速率与C分解的速率相等
B.A、B、C的浓度相等
C.单位时间生成nmolA,同时生成2nmolC
D.A、B、C的分子数之比为1:3:2
【答案】C
【解析】
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)![]() 2C(g),若达到了平衡状态,各组分的浓度不变,正逆反应速率相等。
2C(g),若达到了平衡状态,各组分的浓度不变,正逆反应速率相等。
A. 生成B的速率与C分解的速率均为逆速率,且不等于计量数之比,不是平衡状态,故A不选;
B.各组分的浓度相等,不能证明各组分的浓度不变,无法判断是否达到了平衡状态,故B错误;
C.单位时间生成nmolA是逆速率,同时生成2nmolC是正速率,且等于计量数之比,表明正逆反应速率相等,各组分的浓度不变,达到了平衡状态,故C正确;
D.A、B、C的分子数之比为1:3:2,各组分的分子数之比,无法判断各组分的浓度是否变化,无法判断是否达到平衡状态,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】用如图所示的装置(夹持与加热仪器省略)进行实验,将A中浓硫酸逐滴加入B中(放有木炭),回答下列问题:

(1)图中C装置在实验中的作用是____________。
(2)木炭与浓硫酸反应的化学方程式为____________。
(3)产生的气体通往D中,下列有关实验现象或结论正确的是____________。
A.若D中放有足量的BaCl2溶液,可以产生两种白色沉淀
B.若D中放有足量的Ca(OH)2溶液,可以产生两种白色沉淀
C.若D中放有少量的KMnO4溶液,一段时间后溶液褪色,可证明木炭与浓硫酸反应,有漂白性气体生成
D.若D中放有少量紫色石蕊溶液,一段时间后,溶液先变红色后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用如图所示的装置,进行CO还原Fe2O3的实验(固定装置略)。
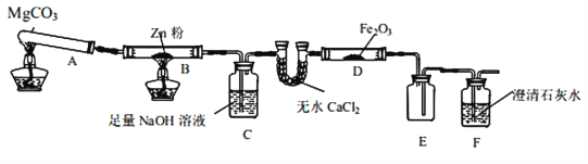
(1)装置B中发生的化学方程式________________。装置C的作用是__________________________
(2)用酒精喷灯对装置D加热,得到灰黑色粉末用黑色粉末进行以下实验:
步骤 | 操作 | 现象 |
1 | 取灰黑色粉末加入稀硫酸 | 溶解,有气泡 |
2 | 取步骤1中溶液,滴加NaOH溶液后,在空气中,搅拌放置 | 白色沉淀最终变为红褐色 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水至过量 | 先变红,后褪色 |
①得到的灰黑色粉末是________________(填写化学式)。
②步骤2中“白色沉淀最终变为红褐色”的化学反应方程式为_________________。
③步骤4中,溶液变红的原因为_____________________________________________________________;溶液褪色可能的原因______________________________________;验证上述原因的实验操作方法为____________。
(3)上述装置,从实验安全考虑,需要采取的改进措施是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是

A. 有O2放电的a极为电池的负极
B. O2-移向电池的正极
C. b极对应的电极反应为2H2-4e-+2O2-=2H2O
D. a极对应的电极反应为O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 100g46%甲酸(HCOOH)水溶液所含的氧原子数为5NA
B. 标准状况下,18g冰水中共价键的数目为NA
C. 56g铁与71gCl2充分反应,转移电子数目为3NA
D. 7.8gNa2O2与足量的水(H218O)反应生成的氧气所含的中子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.18g/ml,质量分数为36.5%浓盐酸配制250ml0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250ml0.1mol/L的盐酸溶液.应量取盐酸体积_________ml,应选用容量瓶的规格__________________ml。
(2)配制时,其正确的操作顺序是________。
A.用30ml水洗涤烧杯 2﹣3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30ml),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250ml的容量瓶中
D.将容量瓶盖紧、振荡、摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1﹣2cm处
a.BCAFED b.BCFED c.BCAED
(3)操作B中,使用量筒量取液体时视线俯视会造成配制液体浓度__________(偏高、偏低或无影响)。操作E中加水超过刻度线该如何处理?____________
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)?
a.没有进行A操作____________;
b.加蒸馏水时不慎超过了刻度___________;
c.定容时俯视_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO)制备草酸镍晶体(NiC2O4·2H2O)的流程如下:
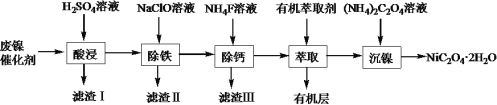
(1)NiC2O4·2H2O中C的化合价是______。既能加快“酸浸”反应速率又能提高“酸浸”原料利用率的操作措施为_____________。
(2)“滤渣Ⅰ”的主要成分是_____________。若控制温度为80℃、pH=2时,“除铁”产生的“滤渣Ⅱ”的主要成分为黄钠铁矾(Na2Fe6(SO4)4(OH)12),写出生成黄钠铁矾沉淀的离子方程式:__________________。
(3)已知“滤渣Ⅲ”的主要成分为CaF2,则“萃取”操作中加入有机萃取剂的作用是__________。
(4)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是_________。
(5)高能锂离子电池的总反应为2Li + FeS = Fe + Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
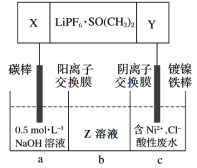
①电极X的反应材料是_________(填化学式);中间隔室b可以得到的主要物质Z是_________(填化学式)。
②电解总反应的离子方程式为_________。已知F=96500C/mol,若电池工作t min,维持电流强度为I A,理论回收Ni_________g(写出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】因存在浓度差而产生电动势的电池称为浓差电池。利用如图所示装置进行实验,开始先闭合K2,断开Kl,电解一段时间后,再断开K2,闭合Kl,形成浓差电池,电流计指针偏转(Ag+浓度越大,氧化性越强)。下列说法不正确的是
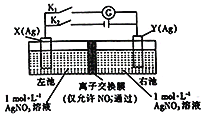
A.闭合K2,断开Kl,NO3-从左池向右池移动
B.断开K2,闭合K1,X为正极
C.闭合K2,断开Kl一段时间后,右池c(AgNO3)增大
D.装置安装后若直接闭合Kl,电流计指针不发生偏转,但往左池加入适当的氨水后,指针偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,E是_________。
(2) 写出C元素基态原子的电子排布式_________________________。
(3)写出D元素原子的价电子排布图____________________。
(4) 元素B与D的电负性的大小关系是___________,C与E的第一电离能的大小关系是___________。(填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com