
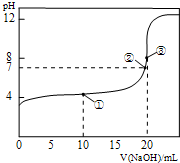
 25℃时,用 0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LCH3COOH溶液所得滴定曲线如图.下列叙述正确的是( )
25℃时,用 0.1000mol/LNaOH溶液滴定20.00mL 0.1000mol/LCH3COOH溶液所得滴定曲线如图.下列叙述正确的是( )| A. | 点①所示溶液:c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| B. | 点②所示溶液:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) | |
| C. | 点③所示溶液:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定终点时:c(CH3COOH)+c(CH3COO-)=c(Na+ ) |
分析 A.点①时,二者反应生成NaAc,还剩余等量的HAc;
B.点②时溶液pH=7,利用电荷守恒来分析;
C.点③时溶液的pH=8,等体积等浓度恰好完全反应,溶质为NaAc,利用水解来分析;
D.由图可知,点③附近达到滴定终点,但溶质可能为NaAc和NaOH.
解答 解:A.点①时,二者反应生成NaAc,还剩余等量的HAc,由物料守恒可知,c(CH3COO-)+c(CH3COOH)=2c(Na+),故A正确;
B.点②时溶液pH=7,则c(H+)=c(OH-),由电荷守恒式为c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则c(Na+)=c(CH3COO-),又显性离子大于隐性离子,则c(Na+)=c(CH3COO-)>c(H+)=c(OH-),故B正确;
C.点③时溶液的pH=8,等体积等浓度恰好完全反应,溶质为NaAc,醋酸根离子水解显碱性,则c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C错误;
D.由图可知,点③附近达到滴定终点,但溶质可能为NaAc和NaOH,则c(CH3COOH)+c(CH3COO-)<c(Na+),故D错误;
故选B.
点评 本题考查酸碱混合的定性判断、离子浓度大小的比较,明确酸碱混合后溶液中的溶质及电荷守恒、物料守恒、水解等即可解答,并注意图象与反应的对应关系来分析解答即可,题目难度中等.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
| 阴离子 阳离子 | OH- | Cl- |
| … | … | … |
| Fe2+ | 不 | ① |
| … | … | … |
| A. | ①处物质的化学式是FeCl2 | B. | ①处物质的名称是氯化铁 | ||
| C. | ①处物质可溶于水 | D. | ①处物质类别属于盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
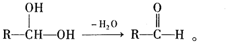
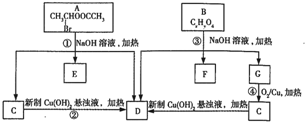



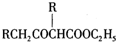 +C2H3OH,请以G为唯一有机试剂合成乙酸乙酯(CH3OCH2COOC2H3),设计合成路线(其他试剂任选),合成路线流程图示例:
+C2H3OH,请以G为唯一有机试剂合成乙酸乙酯(CH3OCH2COOC2H3),设计合成路线(其他试剂任选),合成路线流程图示例: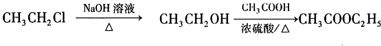
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30 g乙烷中所含的极性共价键数为7NA | |
| B. | 标准状况下,22.4 L N2和CO2混合气体所含的分子数为2NA | |
| C. | 已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,则NA个N2分子与足量氢气充分反应释放热量92.4kJ | |
| D. | Na2O2与CO2反应生成1 molO2时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 10 g H218O中所含的中子数为5NA | |
| B. | 1 mol 铁单质与足量的硫单质充分反应,电子转移数目为3NA | |
| C. | 在1 L 0.1mol/L的NH4Cl溶液中,阴、阳离子总数小于0.2NA | |
| D. | 一定条件下,将1mol N2和3mol H2充分反应,产物分子数目小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
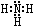 ;B分子也由Z、X两元素组成,作为运送飞船的火箭燃料,常温下是一种液态化合物.已知该化合物的相对分子质量为32,其中X元素的质量分数为12.5%,且该分子结构中只有单键.则B的结构式为
;B分子也由Z、X两元素组成,作为运送飞船的火箭燃料,常温下是一种液态化合物.已知该化合物的相对分子质量为32,其中X元素的质量分数为12.5%,且该分子结构中只有单键.则B的结构式为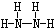 .若64g B分子与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000kJ的热量,写出该反应的热化学方程式N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500kJ/mol.
.若64g B分子与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000kJ的热量,写出该反应的热化学方程式N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
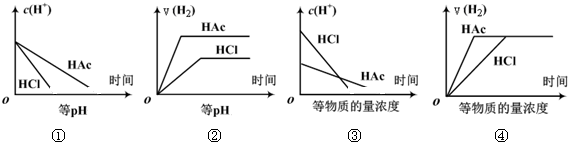
| A. | ①③ | B. | ②④ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | M=WNA | B. | M=$\frac{16w}{b}$ | C. | M=$\frac{w}{16b}$ | D. | M=$\frac{w}{{N}_{A}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X溶液 | 固体Y |  |
| A | 浓硫酸 | 铜粉 | |
| B | 浓氨水 | CaO | |
| C | 稀盐酸 | 石灰石 | |
| D | 浓盐酸 | 高锰酸钾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com