
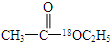 .写出有关反应的化学方程式.
.写出有关反应的化学方程式.| 催化剂 |
| 催化剂 |
| Cu |
| △ |
| 催化剂 |
| 浓硫酸 |
| △ |
| 催化剂 |
| 催化剂 |
| Cu |
| △ |
| 催化剂 |
| 浓硫酸 |
| △ |


科目:高中化学 来源: 题型:
| A、Fe与Cl2反应生成FeCl3,Fe与S反应生成FeS,确定非金属性:Cl>S |
| B、用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜、镁的金属活动性强弱 |
| C、进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 |
| D、测定NaCl和NaF溶液的pH,确定F、Cl两元素非金属性的强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸 | B、硝酸钾 |
| C、氯化钡 | D、氯化铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率增大 |
| C、平衡逆向移动 |
| D、C的体积百分含量增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气与氮气能够缓慢地反应生成氨气,使用合适的催化剂可以提高化学反应速率 |
| B、等质量的锌粉和锌片与相同体积、相同浓度的盐酸反应,反应速率相等 |
| C、用铁片与硫酸制备氢气时,浓硫酸可以加快产生氢气的速率 |
| D、增大反应CO2(g)+H2(g)═CO(g)+H2O(g)的压强,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
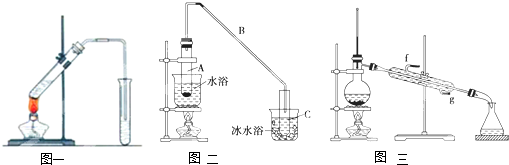
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:
某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:
| 实验目的 | 实验步骤 | 实验现象 | 结论 |
| 验证猜想1 | 1.将一小块钠从煤油中直接取出加热燃烧 2.取出一小块切去表皮并擦干净煤油的钠加热燃烧 | 黑色物质中含 有碳单质 | |
| 验证猜想3 | 黑色物质中 含有铁元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液).
为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCN溶液 |
| B、HF溶液 |
| C、CH3COOH溶液 |
| D、HNO2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com