
【题目】下列分离方法与溶解度有关的是
A.升华B.萃取C.凝华D.磁铁吸引
 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是

A. 用图①装置实现铁上镀铜,a 极为铜,电解质溶液可以是CuSO4溶液
B. 图②装置盐桥中 KCl的 Cl-移向乙烧杯
C. 图③装置中钢闸门应与外接电源的负极相连获得保护
D. 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是( )

A. K1闭合,铁棒上发生的反应为2H++2e-→H2↑
B. K1闭合,石墨棒周围溶液pH逐渐升高
C. K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D. K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25 ℃时0.1 mol·L-1的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中![]() ________(填“增大”、“减小”或“不变”)。
________(填“增大”、“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:__________;所得溶液的pH________7(填“>”、“<”或“=”),用离子方程式表示其原因:__________;所得溶液中各离子物质的量浓度由大到小的顺序是____________________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH![]() )=a moL.L-1,则c(SO42-)为________。
)=a moL.L-1,则c(SO42-)为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用两根金属铂做电极,以KOH溶液做电解质溶液,从两极分别通入CH4(g)和O2,则对该燃料电池的下列叙述中正确的是 ( )
A. 负极的电极反应式为:CH4—8e-+10OH-=CO32-+7H2O
B. 负极的电极反应式为:4OH--4e-=2H2O+O2↑
C. 标准状况下,通入5.6 LO2并完全反应后,有2.00mol电子转移
D. 放电一段时间后,通入O2的电极附近溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
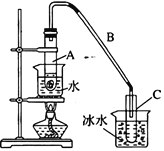
【题目】某化学小组采用类似制乙酸乙酯的装置(如右图所示),用环己醇制备环己烯。
已知: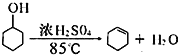
相对分子质量 | 密度/g cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 82 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品
将12.5 mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①在试管中混合环已醇和浓硫酸操作时,加入药品的先后顺序为_________。
②如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_________(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
③将试管C置于冰水中的目的是_______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在__________________层(填“上”或“下”),分液后用__________________(填字母)洗涤。
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
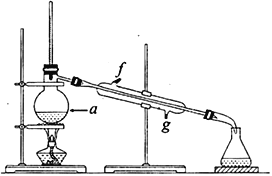
②再将提纯后的环己烯按如图所示装置进行蒸馏。图中仪器a 的名称是_______________。实验中冷却水从__________(填字母)口进入。蒸馏时要加入生石灰,目的是__________________________。
(3)若在制备粗品时环已醇随产品一起蒸出,则实验制得的环己烯精品质量__________(填“高于”、“ 低于”)理论产量。本实验所得到的环已烯质量为6.25g,则产率是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物是天然物质中最多的一类物质,有些具有较强的香气和生理活性。某些萜类化合物可以相互转化。下列说法错误的是
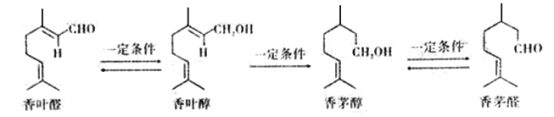
A. 香叶醛的分子式为C10H16O
B. 香叶醇和香茅醛互为同分异构体
C. 上述四种物质均能使酸性高锰酸钾溶液或溴水褪色
D. 香茅醇可以发生取代反应加成反应及氧化反应,但是不能发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.1 mol·L-1的盐酸中逐滴加入0.1 mol·L-1的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述正确的是
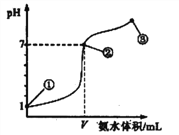
A. V=20mL
B. 在点①所示溶液中:c(Cl-)=c(H+)
C. 在点②所示溶液中:c(H+)=c(NH3·H2O)+c(OH-)
D. 在点②、③之间可能存在:c(NH4+)>c(Cl-)=c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com