
对于平衡体系mA(g)+nB(g) 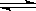 pC(g)+qD(g) 按题目的要求写出可能采取的措施。
pC(g)+qD(g) 按题目的要求写出可能采取的措施。
(1)正、逆反应速率都改变,但平衡不移动,则改变的条件可能是:① ,②若 ,则改变的条件是压强。
(2)只改变正反应速率或只改变逆反应速率,则改变的条件可能是单独改变 或是单独改变 。
(3)正、逆反应速率发生不同程度的变化,则改变的条件可能是:① ,②若 ,则改变的条件是压强。
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源:2016届河南省开封市高三上学期第一次模拟理综化学试卷(解析版) 题型:选择题
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为m g,则该混合物
A.所含碳原子总数为m NA/14
B.所含碳氢键数目为3m NA/14
C.所含公用电子对数目为(m/14+1)NA
D.完全燃烧时消耗的O2一定是33.6m/14 L
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期期中考试化学试卷(解析版) 题型:选择题
全钒液流电池是一种新型的绿色环保储能电池,该电池性能优良,其电池总反应为:v3++VO2++H2O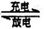 VO2++2H++V2+。下列叙述正确的是
VO2++2H++V2+。下列叙述正确的是
A.充电时阳极附近溶液的酸性减弱
B.充电时阳极反应式为:VO2++2H++e-=VO2++H2O
C.放电过程中电解质溶液中阳离子移向负极
D.放电时每转移1mol电子,负极有1mol V2+被氧化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:填空题
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:CO(g)+2H2(g)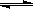 CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数
CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数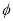 (CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)
(CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)

(2)若在230℃时,平衡常数K=1。若其它条件不变,将温度升高到500℃时,达到平衡时,K 1。
(3)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的 倍。
(4)利用甲醇燃料电池设计如图所示的装置:
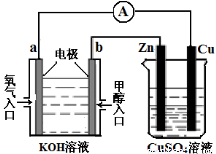
①则该装置中b为 极。
②当铜片的质量变化为12.8 g时,a极上消耗的O2 在标准状况下的体积为 L。
(5)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)== C2H4(g)+3O2(g) ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l)== C2H5OH(1)+3O2(g) ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇反应的热化学方为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上12月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-)
B.一定量的(NH4)2SO4与NH3·H2O混合所得的酸性溶液中:c(NH)<2c(SO)
C.物质的量浓度均为0.01 mol·L-1的CH3COOH和CH3COONa的溶液等体积混合后溶液中c(CH3COOH)+c(CH3COO-)=0.02 mol·L-1
D.物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中c(NH):①>②>③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
已知反应A+B=C+D为放热反应,对该反应的下列说法正确的是
A.A的能量一定高于C
B.B的能量一定高于D
C.A和B的能量总和一定高于C和D的能量总和
D.因该反应为放热反应,故不必加热就可自动进行
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
已知Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是
A.Al2S3、FeS和S B.Fe(OH)3和Al(OH)3
C.Fe2S3和 Al(OH)3 D.FeS、Al(OH)3和S
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
一定条件下反应2AB(g)  A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A.单位时间内生成n molA2,同时消耗2n molAB
B.容器内三种气体AB、A2、B2共存
C.容器中各组分的体积分数不随时间变化
D.AB的消耗速率等于A2的消耗速率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省杭州市五校联盟高三12月月考化学试卷(解析版) 题型:填空题
硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个有一个奇迹。
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在H2的保护下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,写出该反应的化学方程式 。
(2)一种用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的工艺主要流程如下:
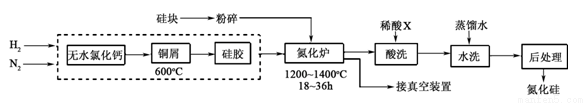
①净化N2和H2时,铜屑的作用是: ;硅胶的作用是 。
②在氮化炉中3SiO2(s)+2N2(g)=Si3N4(s) △H=-727.5kJ/mol,开始时为什么要严格控制氮气的流速以控制温度 ;体系中要通入适量的氢气是为了 。
③X可能是 (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(3)工业上可以通过如下图所示的流程制取纯硅:
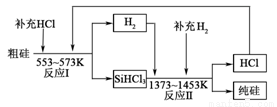
①整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应,写出该反应的化学方程式 。
②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com