
����Ŀ�������£����������ı�0.1mol��L-1��Ԫ����H2C2O4��Һ��pH����Һ�е�H2C2O4��HC2O4-��C2O42-�����ʵ���������(X)��pOH�ı仯��ͼ��ʾ����֪pOH=-lgc(OH-)��![]() ����������������ǣ� ��
����������������ǣ� ��
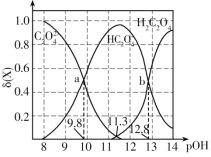
A.��ӦH2C2O4+C2O42-![]() 2HC2O4-��ƽ�ⳣ����ֵΪ103
2HC2O4-��ƽ�ⳣ����ֵΪ103
B.�������¶ȣ�a���ƶ���������
C.pH=3ʱ��![]() =100.6��1
=100.6��1
D.���ʵ���Ũ�Ⱦ�Ϊ0.1mol��L-1��Na2C2O4��NaHC2O4�����Һ�У�c(Na+)>c(C2O42-)>c(HC2O4-)>c(H+)>c(OH-)
���𰸡�B
��������
A����ӦH2C2O4+C2O42-![]() 2HC2O4-��ƽ�ⳣ��K=
2HC2O4-��ƽ�ⳣ��K=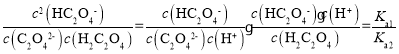 ��a��c(C2O42-)= c(HC2O4-)����ʱpOH=9.8����c(OH-)=10-9.8mol/L��c(H+)=10-4.2mol/L����Ka2=
��a��c(C2O42-)= c(HC2O4-)����ʱpOH=9.8����c(OH-)=10-9.8mol/L��c(H+)=10-4.2mol/L����Ka2=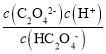 = 10-4.2��ͬ��b��c(HC2O4-)=c(H2C2O4)�ɵ�Ka1=10-1.2�����Է�Ӧ��ƽ�ⳣ��K=
= 10-4.2��ͬ��b��c(HC2O4-)=c(H2C2O4)�ɵ�Ka1=10-1.2�����Է�Ӧ��ƽ�ⳣ��K=![]() ����A��ȷ��
����A��ȷ��
B���¶����ߣ�ˮ�ĵ���̶�����ˮ�����ӻ����pH��pOH֮��С��14����ͼ�����彫�����ƶ�����B����
C��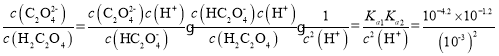 =100.6��1����C��ȷ��
=100.6��1����C��ȷ��
D��H2C2O4��Ka1=10-1.2��Ka2=10-4.2����HC2O4-��ˮ��ƽ�ⳣ��Kh1=![]() ���������̶ȴ�����ˮ��̶ȣ����Դ�NaHC2O4��Һ��c(C2O42-)>c(H2C2O4)����������ʵ���Ũ��Na2C2O4�������ƻ�����������C2O42-������Һ�д���c(C2O42-)>c(HC2O4-)����ͼ��֪��c(C2O42-)>c(HC2O4-)ʱ��Һ�����ԣ������Ӳ�ˮ�⣬���Ի����Һ������Ũ�ȴ�С��ϵΪc(Na+)>c(C2O42-)>c(HC2O4-)>c(H+)>c(OH-)����D��ȷ��
���������̶ȴ�����ˮ��̶ȣ����Դ�NaHC2O4��Һ��c(C2O42-)>c(H2C2O4)����������ʵ���Ũ��Na2C2O4�������ƻ�����������C2O42-������Һ�д���c(C2O42-)>c(HC2O4-)����ͼ��֪��c(C2O42-)>c(HC2O4-)ʱ��Һ�����ԣ������Ӳ�ˮ�⣬���Ի����Һ������Ũ�ȴ�С��ϵΪc(Na+)>c(C2O42-)>c(HC2O4-)>c(H+)>c(OH-)����D��ȷ��
�ʴ�ΪB��


 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڶ��̼������Һ�ڲ�DZˮ�ζ�����ѧ��Ԥ����̼������ܳ�ΪѪҺ���Ʒ��ȫ������(C3F8)��һ�ֳ����Ķ��̼������жԸ����ʵ������в���ȷ����(����)
A. ԭ�Ӱ뾶C��F�Ĵ�
B. ȫ������ĵ���ʽΪ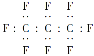
C. ȫ�����������ֻ���Ҽ�
D. ȫ����������мȺ����Լ��ֺ��Ǽ��Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ������ȡSO2����֤SO2��ijЩ���ʵ�װ�ã���ش�
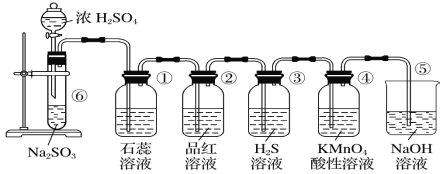
��1���ڢ��з�����Ӧ�Ļ�ѧ����ʽΪ________��
��2�����е�ʵ������Ϊʯ����Һ__________��֤��SO2��ˮ��Һ��_______�ԡ�
��3�����е�Ʒ����Һ________��֤��SO2��________�ԡ�
��4�����е�ʵ��������________________________��֤��SO2��____________�ԡ�
��5�����е�ʵ��������______��֤��SO2��______�ԡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����![]()
![]()
A.NH3��Һ�����������������
B.�����£�������������������ʢװŨ�����Ũ����
C.��������ֽ⣬��������̬����ʱҪ�ܷⱣ�棬����������ͨ�紦
D.�������Ӧʱ��ϡHNO3���ܱ���ԭΪ���ͼ�̬����ϡHNO3������ǿ��ŨHNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ����������Ƽ�ȩ(NaHSO2��HCHO��2H2O)�IJ������£�����ƿ�е�����������Һͨ��SO2�Ƶ�NaHSO3����װ��A�е����ܻ�����Ƥ�����ټ���п�ۺͼ�ȩ��Һ����80��90���£���ӦԼ3h����ȴ�����£����ˣ�����Һ�����������������Ũ������ȴ�ᾧ������˵��������ǣ� ��
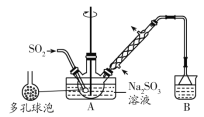
A.�����������ƹ����70%��������ȡ������������
B.������ݵ�������������������Һ�ĽӴ������ʹ��Ӧ��ֽ���
C.װ��B���Լ�������NaOH��Na2CO3��Һ
D.װ��A�пɲ�����ԡ��ɳԡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС������ʵ����̽�����������ʼ�ģ�ҵ��ȡƯ���������ͼװ�ý���ʵ�飺
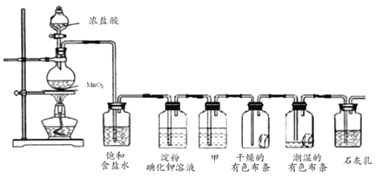
�밴Ҫ��ش��������⣺
��1��Բ����ƿ���������Ļ�ѧ����ʽ________��
��2�����۵⻯����Һ�й۲쵽��������________��
��3�����������ɫ��������ɫ��ʪ����ɫ������ɫ�������ʢ��________��
��4��![]() ��ʯ���鷴Ӧ��ȡƯ�۵Ļ�ѧ����ʽΪ________��
��ʯ���鷴Ӧ��ȡƯ�۵Ļ�ѧ����ʽΪ________��
��5�����������ַ�����ȡ���������ú��Ȼ���146g��Ũ�����������Ķ������̷�Ӧ������87g����������������Ũ���ᷴӦ������������________��
A.�ڱȢٶ� B.�ٱȢڶ� C.һ���� D.���Ƚ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ����������ȼ�ϵ�أ���������Һ�����ԣ���֪��CH2O��n��̼�Ļ��ϼ�Ϊ0�ۣ��йظõ�ص�˵����ȷ����

A. �ŵ�����������Һ��pH����
B. ������22gCO2ʱ��������Ǩ�����ӵ����ʵ���Ϊ4mol
C. ����22gCO2ʱ��Ĥ�����Һ�������仯Ϊ��89g
D. ���������·����������Ϊ��a��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ�¡�ͬѹ�£��������NH3��CH4�������壬�����й�˵��������ǣ���
A.����������Ŀ��ͬB.����֮��Ϊ16��17
C.������ԭ�����ʵ���֮��Ϊ3��4D.�ܶ�֮��Ϊ17��16
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������4 mol HNO3��1 mol H2SO4�Ļ����Һ��������������������Һ�н���������a��b���������۵����ʵ����Ĺ�ϵ��ͼ��ʾ(��֪ϡ����Ļ�ԭ����ֻ��NO)��
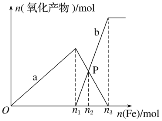
(1)b��ʾ�Ĺ�ϵ����_______(�����ӷ���)
(2)n1��______
(3)P��ʱ��n(Fe2��)��______mol
(4)��P����Һ�м���ͭ�ۣ������ܽ�________g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com