
| A. | 煤炭 | B. | 核能 | C. | 风能 | D. | 氢能 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. |  | B. | 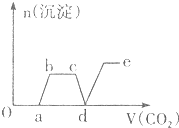 | ||
| C. | 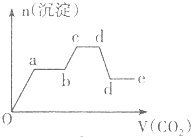 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;由D→E的反应类型是还原反应.
;由D→E的反应类型是还原反应. .
. .
. 为原料,制备化合物
为原料,制备化合物 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
| 1.4×10-3 | 2.55×10-2 | 9×10-4 | 1.1×10-2 |
| A. | 硫酸钙悬浊液中存在CaSO4(s)?Ca2+(aq)+SO42-(aq) | |
| B. | 用Na2CO3溶液浸泡锅炉中的水垢,可将水垢中的CaSO4转化为CaCO3 | |
| C. | 向Mg(OH)2悬浊液中滴加FeCl3,沉淀变为红褐色,说明溶解度Fe(OH)3<Mg(OH)2 | |
| D. | 向2ml饱和MgCl2 溶液中先后滴加0.1mol/L的Na2CO3、NaOH溶液各2滴,产生的白色沉淀为Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L1mol/L的氯化钠溶液中取出10ml后,其浓度仍是1mol/L | |
| B. | NaHSO4溶液与NaOH溶液反应的离子方程式:H++OH-=H2O | |
| C. | FeCl3溶液呈电中性,Fe(OH)3胶体带正电 | |
| D. | 氧化剂具有氧化性,是得到电子(或电子对偏向)的物质,反应时本身被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于10s | B. | 等于10s | C. | 大于10s | D. | 等于5s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x+y<z | B. | 平衡向逆反应方向移动 | ||
| C. | B的转化率降低 | D. | C的体积分数变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 平衡后CO的体积分数为40% | B. | 平衡后CO的转化率为25% | ||
| C. | 平衡后水的转化率为50% | D. | 平衡后水的体积分数为30% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2+O2$?_{加热}^{催化剂}$2SO3△H=-196.6 kJ/mol | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ/mol | |
| C. | 2H2( g )+O2(g)═2H2O (l)△H=+571.6 kJ/mol | |
| D. | C(s)+O2(g)═CO2(g)△H=+393.5 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com