
| A. | 1 mol氧气中含有1.204×1024个氧原子,在标准状况下占有体积22.4 L | |
| B. | 1 mol臭氧和1.5 mol氧气含有相同的氧原子数 | |
| C. | 当He、H2、O2三种气体的温度和密度都相同时,它们的压强大小是p(O2)>p(He)>p(H2) | |
| D. | 等物质的量的干冰和葡萄糖(分子式为C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3 |
分析 A.依据n=$\frac{N}{{N}_{A}}$=$\frac{V}{Vm}$判断;
B.依据N=nNA结合臭氧为三原子分子,氧气为双原子分子解答;
C.在温度和密度都相同条件下,压强与摩尔质量呈反比.据此判断;
D.1个二氧化碳含有1个碳原子和2个氧原子,1个葡萄糖分子含有6个碳原子和6个氧原子.
解答 解:A.氧气为双原子分子,1 mol氧气中含有1mol×2×6.02×1023mol-1=1.204×1024个氧原子,在标准状况下占有体积为:1mol×22.4L/mol=22.4L,故A正确;
B.1 mol臭氧含有氧原子个数为:1mol×3×NA=3NA,1.5 mol氧气含有的氧原子数为1.5mol×2×NA=3NA,所以二者含有相同的氧原子,故B正确;
C.Ne的摩尔质量为4g/mol,H2的摩尔质量为2g/mol,O2的摩尔质量为32g/mol,在温度和密度都相同条件下,压强与摩尔质量呈反比,摩尔质量越大,压强越小,所以三种气体的压强(p)从大到小的顺序是p(H2)>p(Ne)>p(O2),故C错误;
D.1个二氧化碳含有1个碳原子和2个氧原子,1个葡萄糖分子含有6个碳原子和6个氧原子,则等物质的量的干冰和葡萄糖(分子式为C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3,故D正确;
故选:C.
点评 本题阿伏伽德罗常数的综合应用,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间关系是解题关键,注意物质的结构与组成,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
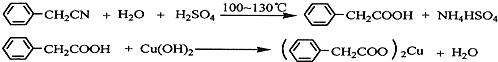
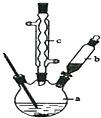
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
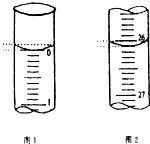 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熵变小于零而焓变大于零的反应肯定不能自发发生 | |
| B. | 热化学方程式中△H的值与反应物的用量有关 | |
| C. | 化学反应中旧键断裂吸收能量,新键形成释放能量,所以化学反应伴随能量变化,但反应前后物质的总能量不变 | |
| D. | 其他条件不变,增大反应物浓度是通过增大活化分子百分数,使化学反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在相同温度下,饱和溶液一定比不饱和溶液导电性强 | |
| B. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| C. | 晶体NaCl不导电,所以它不是电解质,而铜、铁等金属能导电,所以它们是电解质 | |
| D. | 氯化氢溶于水能导电,但液态氯化氢不导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 交警检查司机是否酒后驾车的原理中体现了乙醇的还原性 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同位素 | |
| C. | 铜的金属活动性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| D. | 以石油、煤和天然气为原料通过聚合反应可以获得用途广泛的高分子合成材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com