
| A、用分液漏斗分离乙醇和水 |
| B、用蒸馏的方法将自来水制成蒸馏水 |
| C、用加热的方法分离氯化钠和硝酸钾固体 |
| D、用四氯化碳萃取碘的饱和水溶液中的碘 |


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
 碳及其化合物在人类生产、生活中的应用非常广泛.“低碳生活”不再只是一种理想,更是一种值得期待的生活方式.
碳及其化合物在人类生产、生活中的应用非常广泛.“低碳生活”不再只是一种理想,更是一种值得期待的生活方式.| 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |||
| H2O | CO | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 0.4 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9gD2O所含有的质子数为5NA |
| B、100mL1mol?L-1AlCl3溶液中含的阳离子数大于0.1NA |
| C、25℃时,pH=12的1.0 L NaClO溶液中水电离出的OH-的数目为0.01 NA |
| D、7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
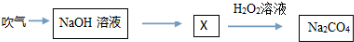
| A、Na2CO4是一种盐,其中碳为+6价 |
| B、X溶液中可能含两种盐 |
| C、该过程中没有发生氧化还原反应 |
| D、NaHCO3与盐酸和氢氧化钠均能反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1.0 | 2.0 | 3.0 | |
| 810 | 54.0 | - | a |
| 915 | - | 75.0 | - |
| 1000 | - | b | 83.0 |
| A、△S<0 |
| B、915℃2.0MPa,A的转化率为60% |
| C、a>b |
| D、平衡常数:K(1000℃)<K(810℃) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
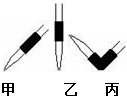 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 23.54 | 20.00 |
| 2 | 0.10 | 23.96 | 20.00 |
| 3 | 0.10 | 24.00 | 20.00 |
| 4 | 0.10 | 24.04 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
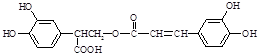
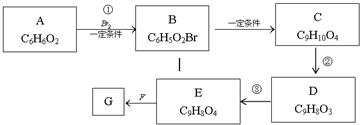
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com