
| A�� | X��Y��Z�����ڱ��в����ܴ���ͬһ���� | |
| B�� | ԭ������Y��X��Z | |
| C�� | �����Ӱ뾶��r��X2-����r��Y+�� | |
| D�� | Y ������X�����е�ȼ���������Ӹ���֮��Ϊ1��1 |
���� ��������Ԫ��ԭ�ӵĵ�������Ϊ25����Z��Y��ԭ������֮�ͱ�X��ԭ��������2������1������Xԭ�ӵ�������Ϊx��Yԭ�ӵ�������Ϊy���������⣬�ɵó����¹�ϵ��
$\left\{\begin{array}{l}{6+x+y=25}\\{6+y=2x+1}\end{array}\right.$
��ã�x=8��y=11����XΪ��Ԫ�أ�YΪ��Ԫ�أ��Ƴ�ZΪ̼Ԫ�أ�Y2X��ZX2�ֱ���Na2O��CO2��Na2O��ˮ�������������ƣ����������������̼��Ӧ����̼���ƣ�
��� �⣺���ݷ����ó���XΪ��Ԫ�أ�YΪ��Ԫ�أ�ZΪ̼Ԫ�أ�
A�������ơ�̼����ͬһ���ڣ���A��ȷ��
B��X������8�ţ���Y���ƣ�11�ţ���Z��̼��6�ţ�����ԭ�������Ӵ�СΪ��Y��X��Z����B��ȷ��
C��X2-ΪO2-��Y+ΪNa+�����Ӳ�ṹ��ͬ��ԭ������С�뾶��������r��X2-����r��Y+������C��ȷ��
D��Y�����ǽ����ƣ�X�������������ڵ�ȼ�����������ɹ������ƣ�Na2O2����������������֮��Ϊ2��1����D����
��ѡ��D��
���� ���⿼��λ�ýṹ���ʵ����ϵӦ�ã���Ŀ�Ѷ��еȣ�����ע����ս�����ϵʽ�ƶ�Ԫ�ص����࣬ѧϰ��ע�ذ���Ԫ�������ɵ���Ҫ���ݣ�


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| �� | �� | �� | �� | |||||
| �� | �� | �� | �� | �� | �� | |||
| �� | �� | �� |
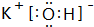 ��
��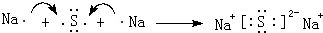 ���û������������ӣ�����ۡ������ӡ��������
���û������������ӣ�����ۡ������ӡ��������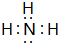 ���û��������ɼ��ԣ�����ԡ��Ǽ��ԡ������γɵģ�
���û��������ɼ��ԣ�����ԡ��Ǽ��ԡ������γɵģ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| ѡ� | ���塡 | �Լ��� | ���� | ���ۡ� |
| ��A | X�����γ����꣩�� | KI������Һ�� | ��Һ������ | X��NO2�� |
| ��B | NH3 | ��̪��Һ | ��Һ���ɫ | ��NH3��ˮ��Һ�Լ��� |
| ��C | Cl2 | ����ɫʯ����Һ | ����Һ������ɫ | Cl2�������ԡ� |
| ��D | SO2 | ��ˮ�� | ��Һ��ɫ�� | SO2��Ư���ԡ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ӵİ뾶��Y��X | |
| B�� | �⻯����ȶ��ԣ�Z��W | |
| C�� | X��Z�γɵĻ���������ˮ������Һ�Լ��� | |
| D�� | Y��W�γɵĻ���������ˮ������Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
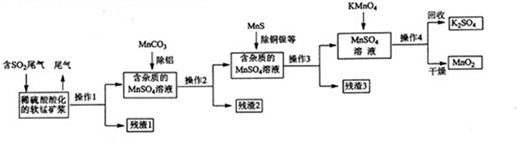
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
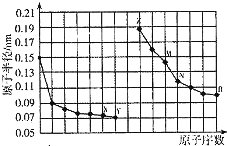
| A�� | NX2һ�������ᷴӦ | |
| B�� | R2��ˮ��Ӧʱ��ˮ�ǻ�ԭ�� | |
| C�� | �����ӵİ뾶��M��Z��X | |
| D�� | ����������Ӧˮ����ļ��ԣ�Z��M |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L 0.1 mol•L-1Na2CO3��Һ�к���0.1NACO32- | |
| B�� | 4.2gN3-�к��еĵ�����Ϊ2.4NA | |
| C�� | 6.4gCu������Ũ���ᷴӦ��һ��ת��0.2 NA������ | |
| D�� | ���³�ѹ�£�22.4L H2O�й��õ��Ӷ���Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
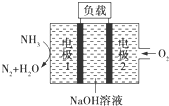
| A�� | ��ع���ʱ��Na+��缫1�ƶ� | |
| B�� | ��ع���һ��ʱ���ֹͣ����ҺpHֵ���� | |
| C�� | �缫1�����ĵ缫��ӦΪ2NH3+6OH--6e-�TN2��+6H2O | |
| D�� | �øõ������Դ��⾫��ͭ��������ÿ����0.2 mol NH3��ͬʱ������õ�19.2g��ͭ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com