
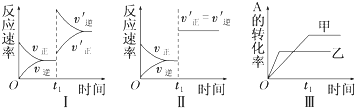
| A. | 图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响 | |
| B. | 图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响 | |
| C. | 图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高 | |
| D. | 图Ⅲ表示的是不同催化剂对平衡的影响,且甲的催化效率比乙高 |
分析 A、增大反应物的浓度,正逆反应速率均增大,但是在增大的瞬间,逆反应速率不变;
B、催化剂只改变反应速率,不影响平衡的移动,对反应前后气体体积不变的反应,增大压强,也只改变反应速率,不影响平衡的移动;
C、升高温度,化学平衡向着吸热方向进行;
D、催化剂只改变反应速率,不影响平衡的移动.
解答 解:A、增大反应物的浓度,正逆反应速率均增大,但是在增大的瞬间,逆反应速率不变,所以逆反应速率在t1时刻不变,不会离开原平衡点,故A错误;
B、催化剂只改变反应速率,不影响平衡的移动,和本图结果一样,该反应前后气体体积不变的反应,增大压强,也只改变反应速率,不影响平衡的移动,和本图结果一样,故B错误;
C、升高温度,化学平衡向着逆方向进行,反应物A的转化率减小,A的转化率在图中是乙<甲,所以乙的温度较高,故C正确;
D、催化剂只改变反应速率,不影响平衡的移动,各物质的转化率不变,故D错误.
故选C.
点评 本题是一道有关化学反应速率和化学平衡知识的图象题,注意固定变量法的运用,难度较大,考查角度广.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素原子核外电子层排布呈周期性变化 | |
| B. | 元素相对原子质量依次递增 | |
| C. | 元素原子半径大小呈周期性变化 | |
| D. | 元素的最高正化合价呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和冷水反应:Na+H2O=Na++OH一+H2↑ | |
| B. | 铁粉投入到硫酸铜溶液中:Fe+Cu2+=Fe2++Cu | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH一=Al(OH)3↓ | |
| D. | 氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子晶体 | B. | 离子晶体 | C. | 分子晶体 | D. | 金属晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 63% | B. | 54% | C. | 12% | D. | 9% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 46:56:27 | C. | 6:3:2 | D. | 1/23:1/28:1/9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A~F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示.
A~F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示.| 元素 | 原子结构或性质 |
| A | 原子最外层电子数是内层电子总数的$\frac{1}{5}$ |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com