
| A.分子晶体中都存在共价键 |
| B.F2、C12、Br2、I2的熔沸点逐渐升高与分子间作用力有关 |
| C.含有极性键的化合物分子一定不含非极性键 |
| D.只要是离子化合物,其熔点一定比共价化合物的熔点高 |
科目:高中化学 来源:不详 题型:单选题
| A.氢键是一种特殊化学键,它广泛地存在于自然界中 |
B.在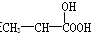 分子中含有1个手性C原子 分子中含有1个手性C原子 |
| C.碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子。 |
| D.含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CO2 | B.N2O | C.CH4 | D.N2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.有些物质是由分子直接构成的,化学式能准确表示该物质分子组成,如白磷(P4)、二氧化碳(CO2)、氯化铵(NH4Cl)等 |
| B.C2H2与BeCl2分子中的中心原子杂化轨道的类型相同 |
| C.在1molSiO2晶体中,含有2molSi-O键 |
| D.二甲苯的沸点顺序是:邻二甲苯>对二甲苯;则羟基苯甲醛的沸点顺序是:邻羟基苯甲醛 >对羟基苯甲醛 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.冰熔化时,分子中H—O键发生断裂 |
| B.原子晶体中,共价键的键长越短,键能越大,熔点就越高 |
| C.分子晶体中,共价键键能越大,该分子的熔沸点就越高 |
| D.分子晶体中,分子间作用力越大,则分子越稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 代号 | 物质 | 结构简式 | 水中溶解度/g (25℃) | 熔点/℃ | 沸点/℃ |
| A | 对—硝基苯酚 | 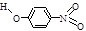 | 1.7 | 114 | 295 |
| B | 邻—硝基苯酚 | 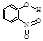 | 0.2 | 45 | 100 |
| | 熔点/K | 沸点/K | 标准状况时在水中的溶解度 |
| 甲 | 187 | 202 | 2.6 |
| 乙 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AlCl3为离子化合物 | B.SiCl4为共价化合物 |
| C.P 与Cl可形成离子键 | D.K与Mg 形成共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com