
| A. | 在离子化合物中一定不存在共价键 | B. | 在单质分子中一定存在共价键 | ||
| C. | 共价键一定只存在于共价化合物中 | D. | 在共价分子中一定存在共价键 |
科目:高中化学 来源: 题型:选择题
| 元素符号 | K | L | M | Q | R | T | N |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
| 主要化合价 | +1 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
| A. | K、L、M三种元素的单质的还原性逐渐增强 | |
| B. | 在RCl2分子中,各原子最外层均满足8电子的稳定结构 | |
| C. | Q元素的最高价氧化物为电解质,其水溶液能够导电 | |
| D. | K在T单质中燃烧所得的化合物中有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
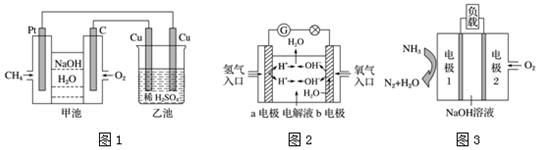
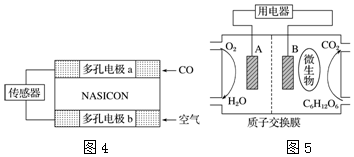
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O、H2S、H2Te分子间作用力依次增大 | |
| B. | 金刚石是碳原子间以共价键相结合的原子晶体,加热熔化时需破坏共价键 | |
| C. | 氢氧化钙和氯化铵固体加热制氨气过程中,均有离子键和共价键的断裂和生成 | |
| D. | SiO2和CO2中每个原子的最外层都具有8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入铝粉能产生H2的溶液:Fe2+、NH4+、SO42-、NO3- | |
| B. | 室温下水电离出c(H+)=1×10-13 mol/L的溶液:HCO3-、K+、SO42-、Cl- | |
| C. | 使酚酞变红色的溶液:Na+、K+、AlO2-、CO32- | |
| D. | 含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
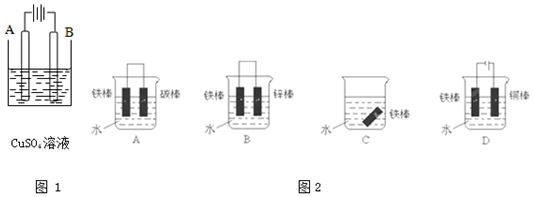
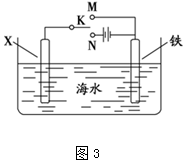
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
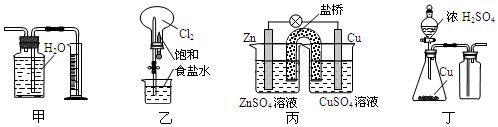
| A. | 用图甲装置收集并测量NO2的体积 | |
| B. | 用图乙装置可以完成“喷泉”实验 | |
| C. | 用图丙装置可以实现化学能转化为电能 | |
| D. | 用图丁装置制取并收集SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com