
氨气是生产氮肥、硝酸、纯碱等的重要原料。
(1)实验室模拟合成氨。在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料(单位是mol /L),平衡时测得甲容器中H2的转化率为20%。
|
|
N2 |
H2 |
NH3 |
|
甲 |
1 |
3 |
0 |
|
乙 |
0.5 |
1.5 |
1 |
|
丙 |
0 |
0 |
4 |
①平衡时甲容器中氨气的浓度为 。
②乙容器中开始反应时,v逆 v正(填<、>或=)。
③达平衡时,甲、乙、丙三容器中NH3的体积分数由大到小的顺序为 。
(2)工业上以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:
2NH3 (g)+ CO2 (g) 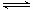 CO(NH2)2
(l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2
(l) + H2O (l),该反应的平衡常数和温度关系如下:
|
T / ℃ |
165 |
175 |
185 |
195 |
|
K |
111.9 |
74.1 |
50.6 |
34.8 |
①焓变ΔH_____0(填“>”、“<”或“=”)。
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) =x,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。
=x,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是 。

③右图中的B点处,NH3的平衡转化率为 。
(9分)(1)①0.4 mol/L(2分) ②>(1分) ③丙>甲=乙(2分)
(2) ①<(1分) ②c(NH3)增大,平衡正向移动(1分) ③32%(2分)
【解析】
试题分析:(1)①氢气的转化率是20%,则甲中消耗氢气的浓度是3mol/L×20%=0.6mol/L,则根据方程式N2+3H2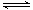 2NH3可知,生成氨气的浓度是0.4mol/L。
2NH3可知,生成氨气的浓度是0.4mol/L。
②乙容器中如果1mol/L氨气完全转化为氮气和氢气,在氮气和氢气的浓度是1mol/L和3mol/L,因此甲和乙容器是等效的。所以乙容器中平衡是氨气的浓度是0.4mol/L,小于1mol/L,因此平衡向逆反应方向进行,即v逆>v正。
③丙容器中相当于氮气和氢气的起始浓度是2mol/L和6mol/L,由于容器体积相等,所以丙容器相当于是在甲容器的基础上增大压强,平衡向生成氨气的方向移动,因此平衡时氨气的体积分数增大,则达平衡时,甲、乙、丙三容器中NH3的体积分数由大到小的顺序为丙>甲=乙。
(2)①根据表中数据可知,随着温度的升高,反应的平衡常数逐渐减小。这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应,则焓变ΔH<0。
②x值越大,即c(NH3)增大,促使平衡向正反应方向移动,因此CO2的转化率增大。
③根据图像可知,B点表示x=4.0,CO2的转化率是64%。设CO2的物质的量是n,则氨气的物质的量是4n。反应中消耗CO2的物质的量=0.64n,则根据方程式可知,消耗氨气的物质的量=0.64n×2=1.28n,因此氨气的转化率=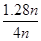 ×100%=32%。
×100%=32%。
考点:考查等效平衡的应用;反应热判断以及可逆反应转化率计算等


科目:高中化学 来源:2011-2012学年广东省中山市高二下学期期末考试化学试卷(带解析) 题型:填空题
(15分)氨气是一种重要的化工原料,大量用于制造尿素、纯碱、铵态氮肥以及硝酸,在有机合成工业中制合成纤维、塑料、染料等。请回答下列问题:
(1)氨气是工业制备硝酸的重要原料,已知下列三个热化学方程式:
① N2 (g)+ 3H2 (g) 2NH3 (g) △H1
2NH3 (g) △H1
② 4NH3(g) +5O2 (g)= 4NO(g) +6H2O(l) △H2
③ N2 (g)+ O2 (g)= 2NO (g) △H
能否应用△H1和△H2表示△H?
若能用△H1和△H2表示△H,则写出△H= ;若不能,说明理由:
。
(2)在相同的温度下,容积相等的两个恒容密闭容器(编号分别为a和b)中,一定量的氮气和氢气发生下列可逆反应:
N2(g) + 3H2(g)  2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
实验测得反应起始时各物质的物质的量及平衡时放出的热量如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 23.1 |
| b | 2 | 6 | 0 | 未知(用E表示) |
 2NH3(g) △H<0 。
2NH3(g) △H<0 。
 CH3OCH3(g)+3H2O(g) △H<0
CH3OCH3(g)+3H2O(g) △H<0| 容器 | c(CO2) /mol·L-1 | c(H2) /mol·L-1 | c(CH3OCH3) /mol·L-1 | c(H2O) /mol·L-1 | v (正)和v (逆)比较 |
| 容器I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v (正)=v (逆) |
| 容器II | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 | |
查看答案和解析>>
科目:高中化学 来源:2013届广东省中山市高二下学期期末考试化学试卷(解析版) 题型:填空题
(15分)氨气是一种重要的化工原料,大量用于制造尿素、纯碱、铵态氮肥以及硝酸,在有机合成工业中制合成纤维、塑料、染料等。请回答下列问题:
(1)氨气是工业制备硝酸的重要原料,已知下列三个热化学方程式:
① N2 (g)+ 3H2
(g)  2NH3 (g) △H1
2NH3 (g) △H1
② 4NH3(g) +5O2 (g)= 4NO(g) +6H2O(l) △H2
③ N2 (g)+ O2 (g)= 2NO (g) △H
能否应用△H1和△H2表示△H?
若能用△H1和△H2表示△H,则写出△H= ;若不能,说明理由:
。
(2)在相同的温度下,容积相等的两个恒容密闭容器(编号分别为a和b)中,一定量的氮气和氢气发生下列可逆反应:
N2(g)
+ 3H2(g)
 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
实验测得反应起始时各物质的物质的量及平衡时放出的热量如下表:
|
容器编号 |
起始时各物质物质的量/mol |
平衡时反应 |
||
|
N2 |
H2 |
NH3 |
||
|
a |
1 |
3 |
0 |
23.1 |
|
b |
2 |
6 |
0 |
未知(用E表示) |
下列说法正确的是 (填序号)
① 反应a和反应b的氢气转化率相同
②利用已知数据可以计算反应b的平衡常数
③利用已知数据可以计算反应b放出的能量E
④平衡时a、b两个反应的氨气体积分数为1:1
(3)温度为400℃、压强为30Mpa的情况下,密闭容器中发生氢气与氮气的合成氨反应:N2(g)+3H2(g)  2NH3(g)
△H<0 。
2NH3(g)
△H<0 。
氨气的物质的量[n(NH3)]和氢气的物质的量[n(H2)]随时间变化的关系如下图:

正反应速率最大的点是 (选填a、b、c、d中的一个或几个),氮气的物质的量[n(N2)]相等的两点是 (选填a、b、c、d中的两个);保持其他条件不变,将温度改为600℃,在上图中画出反应达到平衡的过程中氨气的变化曲线。
(4)工业合成氨用煤制备原料气氢气时,往往排放大量的二氧化碳。实际工业生成中可利用二氧化碳联合生产二甲醚(CH3OCH3),一定条件下,在容积固定的密闭设备中发生反应:
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H<0
CH3OCH3(g)+3H2O(g) △H<0
两个密闭恒容容器中在温度均为T且保持不变的情况下进行上述反应,一段时间后测得两个容器中有关数据及正逆反应速率关系如下表:
|
容器 |
c(CO2) /mol·L-1 |
c(H2) /mol·L-1 |
c(CH3OCH3) /mol·L-1 |
c(H2O) /mol·L-1 |
v (正)和v (逆)比较 |
|
容器I |
1.0×10-2 |
1.0×10-2 |
1.0×10-4 |
1.0×10-4 |
v (正)=v (逆) |
|
容器II |
2.0×10-2 |
1.0×10-2 |
1.0×10-4 |
2.0×10-4 |
|
容器I中的反应 (选填“是”或“否”)达到平衡状态,该反应在温度为T时的平衡常数K= 。表格内的空格处v(正)与v(逆)的大小关系是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气是一种重要的化工原料,主要用于生产氮肥、硝酸、纯碱等化工产品。下图是合成氨,并联合生产硝酸、纯碱的简要流程示意图:
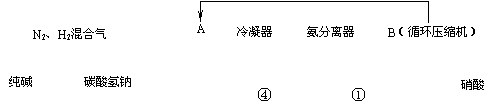 |
(1)设备A的名称是 ,设置循环B→A的目的是 。
(2)反应①的化学方程式是 。
反应③中氧化剂和还原剂的质量比为 。
(3)用两个化学方程式表示过程⑤中的反应过程。
(4)上述纯碱生产中过程⑤CO2的主要来源是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气作为一种重要的化工原料,主要用于生产氮肥、硝酸、纯碱、尿素等化工产品。下图是合成氨,并联合生产硝酸、纯碱、尿素的简要流程示意图:

反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210 | -253 | -78 |
| 沸点(℃) | -195 | -259 | -33 |
(1)设备A的名称是 ,副产物B的化学式是
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。即反应后通过把混合气体的温度至少降低到 ℃(填具体温度),使 分离出来,循环使用的气体有 。
(3)已知尿素的结构简式为![]() 反应②的化学方程式是 。
反应②的化学方程式是 。
|
(5)已知:4NH3+3O2 ![]() 2N2 + 6H2O ,以此设计的氨燃料电池的负极电极反应式为_____________________________(电极材料均为惰性电极,KOH溶液作电解质溶液)。
2N2 + 6H2O ,以此设计的氨燃料电池的负极电极反应式为_____________________________(电极材料均为惰性电极,KOH溶液作电解质溶液)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com