
 Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是
Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
 Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:不详 题型:实验题
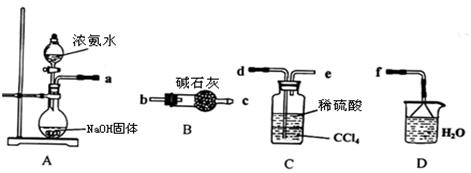
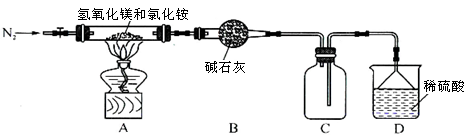
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2O3 + O2,N2O3
N2O3 + O2,N2O3 N2O + O2。在1L密闭容器中加热4molN2O5,达到平衡时,c(O2)为4.5mol?L-1,c(N2O3) 为1.62mol?L-1,则c(N2O5) 为( )
N2O + O2。在1L密闭容器中加热4molN2O5,达到平衡时,c(O2)为4.5mol?L-1,c(N2O3) 为1.62mol?L-1,则c(N2O5) 为( ) | A.1.44mol?L-1 | B.3.48mol?L-1 | C.0.94mol?L-1 | D.1.98mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)+ D(g);ΔH<0,在一定温度和压强下达到平衡。若平衡时C的物质的量与加入B的物质的量的变化关系如图所示。 则下列说法中正确的是
2C(g)+ D(g);ΔH<0,在一定温度和压强下达到平衡。若平衡时C的物质的量与加入B的物质的量的变化关系如图所示。 则下列说法中正确的是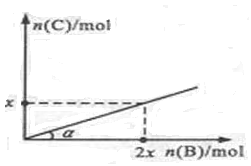
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
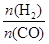 ]:当γ=2时,甲醇的选择性[λ =
]:当γ=2时,甲醇的选择性[λ =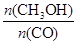 ]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。
]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。| 序号 | 干燥方法 | CO转化率/% |
| ① | 不处理 | 40.2 |
| ② | 无水乙醇洗 | 56.3 |
| ③ | 以四氢呋喃洗 | 62.4 |
| ④ | 无水乙醇洗并真空干燥 | 70.1 |
| ⑤ | | 77.2 |
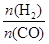 = 2时甲醇合成过程中压力和温度随时间变化的图像。
= 2时甲醇合成过程中压力和温度随时间变化的图像。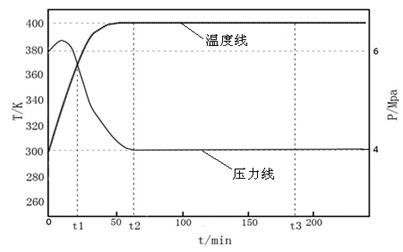
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
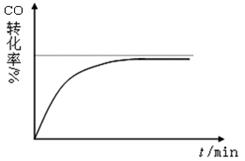
 xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图: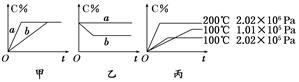
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)(正反应为放热反应),下列说法中正确的是( )
2NH3(g)(正反应为放热反应),下列说法中正确的是( )| A.达到平衡后加入N2,当重新达到平衡时,NH3的浓度比原平衡的大,N2的浓度比原平衡的小 |
| B.达到平衡后,升高温度,既加快了正、逆反应速率,又提高了NH3的产率 |
| C.达到平衡后,缩小容器体积,既有利于加快正、逆反应速率,又有利用提高氢气的转化率 |
| D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大了,而逆反应速率减小了 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com