
【题目】实验室欲快速制取H2,应选用正确的措施是
A.纯锌与稀硫酸反应B.粗锌跟稀硫酸反应
C.粗锌跟硝酸反应D.将浸泡过CuSO4溶液的Zn跟稀硫酸反应
科目:高中化学 来源: 题型:
【题目】(1)H2A在水中存在以下平衡:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。NaHA溶液显酸性,则溶液中离子浓度的大小顺序为__________________________。
H++A2-。NaHA溶液显酸性,则溶液中离子浓度的大小顺序为__________________________。
(2)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)![]() Ca2+(aq)+A2-(aq)滴加少量Na2A固体,c(Ca2+)___(填“增大”“减小”或“不变”),原因是______。
Ca2+(aq)+A2-(aq)滴加少量Na2A固体,c(Ca2+)___(填“增大”“减小”或“不变”),原因是______。
(3)含有![]() 的废水毒性较大,某工厂废水中含4.00×10-3 mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含4.00×10-3 mol·L-1的Cr2O![]() 。为使废水能达标排放,作如下处理:
。为使废水能达标排放,作如下处理:![]()
![]() Cr2+、Fe3+
Cr2+、Fe3+![]() Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
①该废水中加入FeSO4·7H2O和稀硫酸,发生反应的离子方程式为:_______。
②若处理后的废水中残留的c(Fe3+)=1×10-13 mol·L-1,则残留的Cr3+的浓度为__________________。{已知:Ksp[Fe(OH)3]≈1.0×10-38 ,Ksp[Cr(OH)3]≈1.0×10-31}
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯为基础原料,可以合成多种有机物。

回答下列问题:
(1)由苯合成有机物A用到的无机试剂为______________
(2)B分子中的官能团的名称为__________,生成PF树脂的反应类型为_____________
(3)由B生成C的化学方程式为_____________
(4)试剂D可以是___________________(填代号)
a.溴水 b.高锰酸钾溶液 c.Ag(NH3)2OH溶液 d.新制Cu(OH)2悬浊液
(5)写出同时满足下列条件的肉桂酸乙酯的一种同分异构体________________
①苯环上仅有2个取代基且处于对位
②能发生水解反应和银镜反应,其中一种水解产物遇FeCl3溶液显紫色
③为顺式异构
(6)以乙醇为原料合成CH3-CH=CH-COOCH2CH3,其他试剂任选,写出合成路线_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题。
Ⅰ.已知H—H键的键能为436kJ·mol-1,N—H键的健能为391kJ·mol-1,N![]() N键的键能是945.6 kJ·mol-1,则反应NH3(g)
N键的键能是945.6 kJ·mol-1,则反应NH3(g)![]()
![]() N2(g)+
N2(g)+![]() H2(g)的ΔH=______,若在某温度下其平衡常数为K,则N2(g)+3H2(g)
H2(g)的ΔH=______,若在某温度下其平衡常数为K,则N2(g)+3H2(g) ![]() 2NH3(g)的平衡常数K1=___________(用K表示)
2NH3(g)的平衡常数K1=___________(用K表示)
Ⅱ.氯氨是氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯氨、二氯氨和三氯氨(NH2Cl、NHCl2和NCl3),副产物少于其它水消毒剂。
(1)工业上可利用反应2Cl2(g)+NH3(g)![]() NHCl2 (l)+2HCl(g)制备二氯胺。
NHCl2 (l)+2HCl(g)制备二氯胺。
①二氯氨在中性、酸性环境中会发生强烈水解,生成具有强杀菌作用的物质,写出具有强杀菌作用的物质的电子式_______________________。
②在恒温条件下,将2molCl2和1molNH3充入某密闭容器中发生上述反应,测得平衡时Cl2和HCl的物质的量浓度与平衡总压的关系如图所示。则A、B、C三点中Cl2转化率最高的是________点( 填“A” “B”或“C”);计算C点时该反应的压强平衡常数Kp(C)=_____________(Kp是平衡分压代替平衡浓度计算,分压= 总压×物质的量分数。)

(2)用Cl2和NH3反应制备三氯胺的方程式为3Cl2(g)+NH3(g)![]() NCl3(l)+3HCl(g),向容积均为1L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2molCl2和2molNH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
NCl3(l)+3HCl(g),向容积均为1L的甲、乙两个恒温(反应温度分别为400℃、T℃)容器中分别加入2molCl2和2molNH3,测得各容器中n(Cl2)随反应时间t的变化情况如下表所示:
t /min | 0 | 40 | 80 | 120 | 160 |
n(Cl2)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(Cl2)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①T℃__________400℃(填“>”或“<”)。
②该反应的ΔH__________0(填“>”或“<”)。
③该反应自发进行的条件是__________(填高温、低温、任何温度)。
④对该反应,下列说法正确的是_________(填选项字母)。
A.若容器内气体密度不变,则表明反应达到平衡状态
B.若容器内Cl2和NH3物质的量之比为3∶1,则表明反应达到平衡状态
C.反应达到平衡后,其他条件不变,在原容器中按![]() =
=![]() 继续充入一定量反应物,达新平衡后Cl2的转化率增大
继续充入一定量反应物,达新平衡后Cl2的转化率增大
D.反应达到平衡后,其他条件不变,加入一定量的NC13,平衡将向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:
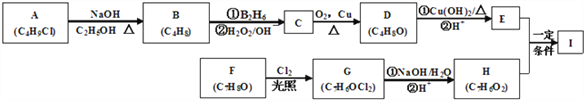
已知以下信息:
A的核磁共振氢谱表明其只有一种化学环境的氢;R—CH=CH2![]() R—CH2CH2OH
R—CH2CH2OH
化合物F苯环上的一氯代物只有两种;通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)C的化学名称为________________________。
(2)E的结构简式为______________________。
(3)A→B的反应类型为_________________、__________________;E+H→I的反应类型为_______________________。
(4)F生成G的化学方程式为____________________________________。
(5)E+H→I的化学方程式为___________________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基;②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,这样的同分异构体共有_______种(不考虑立体异构)。J的一种同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)一定温度下,在容积固定的密闭容器中进行的可逆反应:2NO2![]() 2NO+O2,达到平衡的标志是
2NO+O2,达到平衡的标志是
①相同时间内,氧气的生成速率为n mol·L-1·s-1,NO2的生成速率为2n mol·L-1·s-1
②单位时间内生成n mol O2的同时生成2n mol的NO
③混合气体的颜色不再变化 ④混合气体的密度保持不变
⑤混合气体的平均相对分子质量不再改变 ⑥压强不随时间变化而变化
A. ①③⑤⑥ B. ②③⑤
C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 铝合金是一种混合物,它比纯铝的熔点高
B. 电解熔融三氯化铝可生产金属金属铝
C. 水晶项链和餐桌上的瓷盘都是硅酸盐制品
D. 铜具有良好的导电性,常用来制作印刷电路板
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分).氮化硅(Si3N4)是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上普遍采用高纯硅与纯氮在1300℃反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是 。
A.制汽轮机叶片 | B.制有色玻璃 | C.制永久性模具 | D.制造柴油机 |
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,她不与其他无机酸反应。试推测该陶瓷被氢氟酸腐蚀的化学方程式为 。
(3)现用四氯化硅和氮气在氢气中加强热发生反应,可制得高纯度氮化硅,反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在向盛有氯化铁溶液的烧杯中加入过量铜粉,反应结束后过滤,对溶液中大量存在的金属阳离子的成分判断正确的是
A.只有Cu2+B.Fe2+、Cu2+C.Fe3+、Fe2+D.Fe3+、Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com