


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
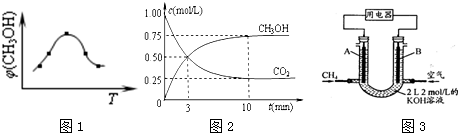
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向硝酸银溶液中加盐酸:Ag++Cl-═AgCl↓ |
| B、向氢氧化钡溶液中加硫酸溶液:SO42-+Ba2+═BaSO4↓ |
| C、向稀硫酸溶液中加铁:2Fe+6H+═2Fe3++3H2↑ |
| D、碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮化硅陶瓷是新型无机非金属材料属共价化合物 |
| B、C60由原子直接组成的晶体,可用于制造纳米材料 |
| C、纤维素、蛋白质、酚醛树脂都属于天然高分子材料 |
| D、单晶硅常用于制造半导体材料和光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:Y>Z>W |
| B、Y的最高价氧化物对应的水化物为强碱 |
| C、对应氢化物的热稳定性:HmZ<HnW |
| D、XW2分子中各原子最外层电子未均达到8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
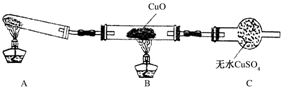
| H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com