
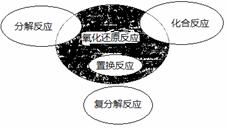
氧化还原反应与四种基本反应类型的关系如图所示。下列化学反应属于阴影部分的是
A.4NH3 +5O2= 4NO + 6H2O
B.4Fe(OH)2 + O2 + 2H2O=4Fe(OH)3
C.2NaHCO3 = Na2CO3 + H2O + CO2↑
D.Cl2 + 2NaBr = 2NaCl + Br2
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
在自然界中,不存在硅单质,它一般是通过硅的氧化物(SiO2)来提取。对制得的粗硅可用以下方法提纯:
Si (粗)+2Cl2 SiCl4 SiCl4+2H2
SiCl4 SiCl4+2H2 Si (纯)+4HCl
Si (纯)+4HCl
(1)写出工业制粗硅的化学方程式________________,该反应的类型为________反应,其中焦炭的作用是________________。
(2)粗硅提纯的两个反应的反应类型分别为________反应,________反应。
(3)SiCl4是一种液体,沸点较低,若从含有粗硅的SiCl4的混合体系中,提取出纯净的SiCl4的方法是________________,该实验方法中所用到的玻璃仪器有________________。
(4)在得到纯硅的反应中,参加反应的SiCl4是气体状态,请回答这样提纯的好处____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种元素原子的核电荷数在10~18之间,它们的最高价氧化物对应水化物是HXO4、H2YO4、H3ZO4。则下列判断正确的是
A.元素电负性:按X、Y、Z变小
B.含氧酸的酸性:H3ZO4>H2YO4>HXO4
C.气态氢化物稳定性:按X、Y、Z顺序增加
D.非金属性:X<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E、F六种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8;E与B的质量比为1:1。F+离子的3d轨道中电子全充满。回答下列问题:
(1)写出基态E原子的电子排布式──────────────── 。
(2)用电子式表示AE2的形成过程 。
(3)B、C两元素的第一电离能大小关系为:───>────(填写元素符号),原因是 。
(4)B元素的最低价氢化物分子立体构型为 。中心原子的杂化方式为 。
(5)向F2+离子的溶液中加入过量CH3的浓溶液,充分反应后溶液呈深蓝色,该反应的离子方程式是__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“纳米材料”(1 nm=10-9m )是指研究开发直径为几纳米至几十纳米的材料。如将“纳米材料”分散到某液体中,对于所得分散系的叙述不正确的是
A.光束通过此分散系时会形成一条光亮的“通路”
B.此分散系中“纳米材料”的粒子在做不停的、无序的运动
C.用滤纸过滤的方法可以从此分散系中分离得到该“纳米材料”
D.在外加电场作用下,“纳米材料”的粒子可能向某一极做定向运动
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制ClO2的化学反应:2NaClO3 + SO2 + H2SO4=2ClO2 + 2NaHSO4,下列说法正确的是
A.NaClO3在反应中化合价降低,失去电子
B.SO2在反应中发生氧化反应
C.1 mol氧化剂在反应中得到2 mol电子
D.H2SO4 在反应中作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填空:
(1)某溶液中只含有K+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
(2)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑,回答下列问题:
①该反应中的氧化剂是_______________。
②用单线桥表示此反应转移的电子数目及方向。
_______________________________________________
③若氧化产物比还原产物多1.75 mol,上述反应转移的电子数目为 。
(3)镁、铝合金3 g与100 mL稀H2SO4恰好完全反应,将反应后所得溶液蒸干,得无水硫酸盐17.4 g,则原硫酸溶液的物质的量浓度为
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如下图),每次实验时,通过灵敏电流计测出电子流动方向如下:
|
| 所用金属 | 电子流向 |
| ① | A、Cu | A→Cu |
| ② | C、D | D→C |
| ③ | A、C | C→A |
| ④ | B、Cu | Cu→B |
| ⑤ | …… | …… |
根据上述情况,回答下列问题:
(1)上述五种金属的活动性顺序是_____________________________。
(2)在①中,Cu片上观察到的现象是:_____________________________;
(3)在②中,溶液中H+向金属片________移动;
(4)在④中,两金属片上均无气泡放出。此时两金属片上的电极反应式分别为:
Cu:____________________________;B:_____________________________;
(5)如果实验⑤用B、D,则导线中电流方向为:_________(填B→D或D→B);
(6)已知反应:Cu+2Fe3+==Cu2++2Fe2+。请用下列试剂和材料,用上图所示装置,将此反应设计成原电池并检验正极产物。
试剂:CuCl2溶液、FeCl3溶液、FeCl2溶液、KSCN溶液、K3[Fe(CN)6]溶液、双氧水、NaOH溶液
材料:Cu片、Fe片、石墨棒
a、设计电池应选用的试剂和材料是:__________________________________;
b、检验正极产物选用的试剂是_______________________,检验反应的离子方程式:
_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将12.8gMg、Al、Fe组成的合金溶于足量的NaOH溶液中,可产生0.3mol气体。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,其质量为38.3g,则上述反应中生成NO气体的体积(标准状况下)为( )
A. 11.2L B. 33.6L C. 22.4L D.6.72L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com