
| A.化学反应的熵变与反应的方向无关 |
| B.化学反应的熵变直接决定了反应的方向 |
| C.熵值增大的反应都是混乱度增大的反应 |
| D.熵值增大的反应都能自发进行 |
科目:高中化学 来源:不详 题型:填空题
 CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。  CO2转化率(%) CO2转化率(%)n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Q(g) ΔH<0的影响。下列有关说法正确的是
2Q(g) ΔH<0的影响。下列有关说法正确的是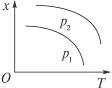
| A.x不可能是M或N的体积分数 |
| B.x可能是混合气体的物质的量 |
| C.该反应在p1时先达到化学平衡状态 |
| D.p 1>p2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.11∶15 | B.小于11∶15 | C.5∶6 | D.大于5∶6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 bR(g)达到平衡后,温度和压强对该反应的影响如下图所示,图中压强p1> p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
bR(g)达到平衡后,温度和压强对该反应的影响如下图所示,图中压强p1> p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( ) 
| A.上述反应是放热反应 | B.上述反应是吸热反应 |
| C.a>b | D.d<b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2NO(g)+O2(g)。将1molNO2、0.2molO2和一定量的NO通入容积为2L的密闭容器内反应,10min后反应恰好达到平衡状态,此时容器内有0.6molNO,容器内压强为原来的8/7。计算:(要求有计算过程)
2NO(g)+O2(g)。将1molNO2、0.2molO2和一定量的NO通入容积为2L的密闭容器内反应,10min后反应恰好达到平衡状态,此时容器内有0.6molNO,容器内压强为原来的8/7。计算:(要求有计算过程)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)+3D(g)的反应,其中A、B、C、D的起始浓度分别为0.1 mol·L-1、0.4 mol·L-1、0.2 mol·L-1、0.3 mol·L-1,当反应达到平衡时,各物质的物质的量浓度不可能是( )
2C(g)+3D(g)的反应,其中A、B、C、D的起始浓度分别为0.1 mol·L-1、0.4 mol·L-1、0.2 mol·L-1、0.3 mol·L-1,当反应达到平衡时,各物质的物质的量浓度不可能是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
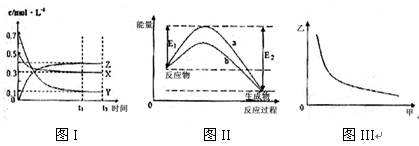

| A.该反应热化学方程式为X(g) +3Y(g) 2Z(g)△H=―(E2―E1) |
| B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线 |
| C.该温度下,反应的平衡常数数值约为533。若升高温度,该反应的平衡常数减小,Y的转化率降低 |
| D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a是没有加入催化剂时的能量变化曲线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com