
| A、生铁与钢的区别在于生铁含碳杂质,而钢不含 |
| B、铜在自然界中的含量高,所以铜是人类最早使用的金属 |
| C、黑色金属材料包括铁、铬、锰及其化合物 |
| D、金属一般都具有导电性、导热性、延展性 |


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
| A、0.1 mol?L-1NH4Cl溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| B、溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) |
| D、25℃时,pH=7的NH4Cl与NH3?H2O混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、易被强氧化剂KMnO4等氧化 |
| B、属于不饱和烃易发生加成反应 |
| C、虽然不饱和但比较易发生取代反应 |
| D、苯是一种重要的有机溶剂可广泛应用于生产绿色油漆等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为: 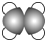 ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为 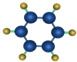 | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与D反应生成相对分子质量为100的酯E | ①由C、H、O三种元素组成; ②球棍模型为 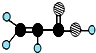 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、饱和氯水中 Cl-、NO3-、Na+、SO32- |
| B、加入甲基橙试液呈红色的溶液 NH4+,K+,SO42-,Cl- |
| C、Na2S溶液中 SO42-、K+、Cl-、Cu2+ |
| D、pH=12的溶液中 NO3-、I-、Na+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定含有I-,不能确定是否含有Cl- |
| B、可能含有NO3-、Cl-和I- |
| C、可能含有NO3- |
| D、一定含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 晶体硅熔点高硬度大 | 可用于制作半导体材料 |
| B | 氢氧化铝具有弱碱性 | 可用于制胃酸中和剂 |
| C | 漂白粉在空气中不稳定 | 可用于漂白纸张 |
| D | 氧化铁能与酸反应 | 可用于制作红色涂料 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下甲烷和氧气的密度之比2:1 |
| B、1g甲烷和1g 氧气的原子数之比为5:1 |
| C、等物质的量的甲烷和氧气的质量之比2:1 |
| D、等质量的甲烷和氧气的体积之比为2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com