
【题目】某同学设计如下装置进行铁与水反应的实验,虚线框处的装置用来检验生成的气体。下列说法正确的是(已知:Fe + 2Fe3+ = 3Fe2+)
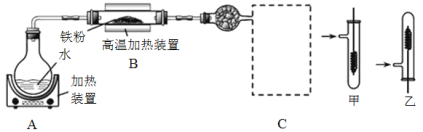
A.实验后,装置B中生成红棕色固体
B.虚线框C处应该选择装置甲
C.实验时将螺旋状铜丝加热变黑后再趁热迅速伸入试管中,可观察到铜丝由黑变红
D.实验后,将装置B中的固体溶于足量稀硫酸,所得溶液中一定含有Fe3+
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,则下列叙述中正确的是
A. 6.02×1022个H2SO分子在水中可电离生成2NA个H+
B. 在0℃、101kPa时,22.4L氢气中含有NA个氢原子
C. 14g氮气中含有7NA个电子
D. NA个一氧化碳分子和0.5mol甲烷的质量比为7︰4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中进行反应:N2+3H2![]() 2NH3。该反应达到平衡的标志是
2NH3。该反应达到平衡的标志是
A.3v(H2)正=2v(NH3)逆B.单位时间生成m mol N2的同时生成3m mol H2
C.混合气体的密度不再随时间变化D.容器内的总压强不再随时间而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒压下,在容积可变的密闭容器中,反应2NO2(g) N2O4(g)达到平衡后,再向容器中通入一定量的NO2,又达到平衡时,N2O4的体积分数( )
A.不变B.增大C.减小D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用铝土矿和硫铁矿烧渣(配料中含Al2O3、Fe2O3、FeO及SiO2等)为原料制备无机高分子絮凝剂聚合碱式氯化铝铁的流程如下:

(提示:SiO2为难溶于盐酸的固体)
(1)配料中属于两性氧化物的是_________________,步骤Ⅱ酸溶时,Al2O3被溶解的离子方程式为___________________________________。
(2)“滤渣1”的主要成分为________(填化学式)。
(3)步骤Ⅳ加入H2O2溶液的目的是__________,发生反应的离子方程式为____________。
(4)步骤Ⅴ加入适量NaOH溶液发生反应生成聚合碱式氯化铝铁,若NaOH过量,可能造成的影响是_________;步骤Ⅵ包含的操作有________、洗涤、干燥。
(5)测定聚合碱式氯化铝铁[FeaAlb(OH)xCly]n中n(Fe)/n(Al)的比值的步骤如下:
步骤1:准确称取产品5.7100g溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到3.3500g固体。
步骤2:另准确称取相同质量样品,溶于足量NaOH溶液,过滤,充分洗涤,将滤渣灼烧至质量不再变化,得到固体0.8000g。
计算产品中![]() 的比值为____________。
的比值为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 为阿伏伽德罗常数的值。已知常温下 1L0.1molL-1NaHSO3溶液的pH=4,该溶液中存在如下平衡:①HSO3-![]() H++SO32- ② HSO3- + H2O
H++SO32- ② HSO3- + H2O![]() H2SO3+ OH-。下列说法正确的是
H2SO3+ OH-。下列说法正确的是
A.将该溶液加热蒸干、灼烧可得NaHSO3固体
B.加水稀释该溶液,平衡①正向移动,溶液中c(H+ )增大
C.该溶液中c(OH-)+ c(SO32-)=c(H+) +c(H2SO3)
D.该溶液中阴阳离子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述正确的是( )
A.化学反应中电子转移的表示方法
B.离子M2O7x-与S2-能在酸性溶液中发生如下反应:M2O7x-+3S2-+14H+=2M3+ +3S +7H2O,则M2O7x-中M的化合价为+7
C.在常温下发生以下几个反应:①16H++10Z-+2XO4-=2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2 =B2+2Z-根据上述反应,可知道氧化性强弱顺序为:XO4->Z2>B2>A3+
D.已知硝酸铵在一定温度下分解为5NH4NO3=4N2↑+2HNO3+9H2O↑,被氧化的元素和被还原的元素的质量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。
(1)当反应达到平衡时,N2和H2的转化率比是_____。升高平衡体系的温度(保持容积不变),混合气体的平均相对分子质量______,密度____。(填“变大”、“变小”或“不变”)
(2)当达到平衡时,充入氩气,并保持压强不变,平衡将______(填“正向”、“逆向”或“不”)移动。若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将_____(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度___(填“大于”、“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图表示AlCl3溶液与NaOH溶液相互滴加过程中微粒的量的关系曲线。下列判断错误的是( )

A. ①线表示Al3+的物质的量的变化
B. x表示AlCl3的物质的量
C. ③线表示Al(OH)3的物质的量的变化
D. ④线表示[Al(OH)4]-的物质的量的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com