
| A、1mol NaHSO4晶体含有2NA个离子 |
| B、1L2mol/L明矾溶液经水解可得到氢氧化铝胶体粒子的数目为2NA个 |
| C、1mol CH3+(碳正离子)中含有的电子数为10NA |
| D、在O2参与的反应中,1molO2作氧化剂时得到的电子数一定是4NA |


科目:高中化学 来源: 题型:
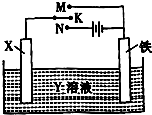 高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=akJ?mol-1
高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=akJ?mol-1| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:丙>丁>乙 |
| B、单质的还原性:丁>丙>甲 |
| C、甲、乙、丙的氧化物均只有一种 |
| D、乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、500mL 2mol?L-1 葡萄糖溶液中所含分子数为NA |
| B、0.1mol?L-1Na2CO3溶液中的阴离子总数大于0.1NA |
| C、电解精炼铜时,若阳极质量减少64g,则外电路导线上不一定通过2 NA个电子 |
| D、标准状况下,22.4L NO和11.2L O2混合后气体的分子总数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,22.4L CO2中含有NA个CO2分子 |
| B、17.6g丙烷中所含的极性共价键为4NA个 |
| C、1.7g H2O2中含有的电子数为0.9NA |
| D、在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在标准状况下,2.24L氮气含有共用电子对数的0.5NA |
| B、22.4g铁粉完全溶于一定浓度的硝酸中,转移的电子数可能为0.6NA |
| C、4.6g甲醇和二甲醚(CH3-O-CH3)的混合物中所含分子数等于0.1NA |
| D、含Al3+数目为0.1NA的硝酸铝溶液中,NO3-个数大于0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
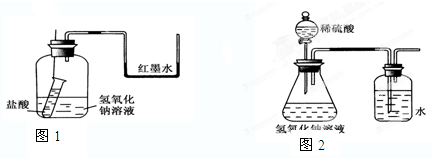
| 编号 | 盐酸 | 氢氧化钠 | △t/℃ |
| 1 | 0.1mol?L-1 | 0.05mol?L-1 | 3.5 |
| 2 | 0.1mol?L-1 | 0.1mol?L-1 | x |
| 3 | 0.2mol?L-1 | 0.2mol?L-1 | 14 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.05mol/L |
| B、0.001mol/L |
| C、0.002mol/L |
| D、0.005mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com