
| A、反应放出的热量为0.04a KJ |
| B、平衡时H2O的转化率为40% |
| C、若将容器的体积压缩为1L,有利于该反应平衡正向移动 |
| D、判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等 |
| 0.08mol |
| 0.2mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、氧化性:I2>Cl2 |
| B、每生成1 mol KIO3转移电子2 mol |
| C、该反应是置换反应 |
| D、反应物和生成物中只含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2ag | ||
| B、(2+S/100)ag | ||
C、
| ||
D、(1+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把浑浊的液体倒入蒸发皿内加热 | ||
| B、开始析出晶体后用玻璃棒搅拌 | ||
C、蒸发时液体不超过蒸发皿容积的
| ||
| D、蒸发皿中出现大量固体时即停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容器里气体的密度为40 g/L |
| B、SO3的分解率为20% |
| C、在这10 min内的平均速率为υ(O2)=0.005 mol?L-1?min-1 |
| D、化学反应速率:υ(Ag2SO4)=υ(SO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应速率与I-浓度有关 |
| B、IO-是该反应的催化剂 |
| C、当反应放出98 kJ的热量时会生成1 mol O2 |
| D、v(H2O2)=v(H2O)=v(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:

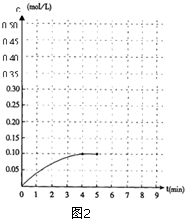 内加入0.2mol的N2和0.6mol 的H2,在一定条件下发生如下反应:N2 (g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化的情况如图2:
内加入0.2mol的N2和0.6mol 的H2,在一定条件下发生如下反应:N2 (g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化的情况如图2:查看答案和解析>>
科目:高中化学 来源: 题型:
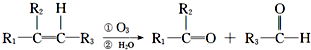
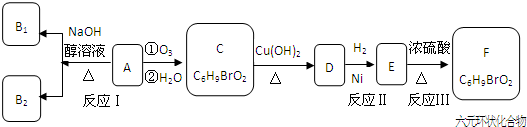
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com