
| A. | (1)和(6) | B. | (3)和(4) | C. | (2)和(4) | D. | (2)和(5) |
分析 (1)离子之间发生氧化还原反应;
(2)酸性条件下Ag(NH3)2+不能大量共存;
(3)离子之间不发生任何反应;
(4)离子之间不发生任何反应;
(5)酸性条件下弱酸的酸根离子不能大量共存;
(6)反应生成沉淀.
解答 解:(1)酸性条件下ClO-、NO3-具有强氧化性,与I-发生氧化还原反应,故错误;
(2)酸性条件下Ag(NH3)2+不能大量共存,故错误;
(3)离子之间不发生任何反应,可大量共存,故正确;
(4)离子之间不发生任何反应,可大量共存,故正确;
(5)酸性条件下弱酸的AlO2-、C6H15O-不能大量共存,故错误;
(6)Pb2+、SO42-反应生成沉淀,不能大量共存,故错误.
故选B.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:推断题
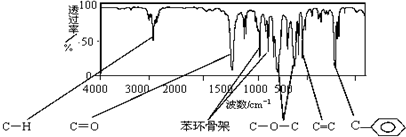
 .
.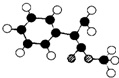 (图中球与球之间连线表示单键或双键).
(图中球与球之间连线表示单键或双键).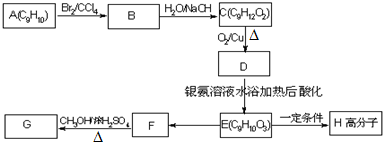
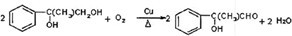 .E→H
.E→H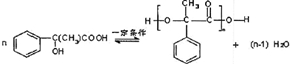 .
.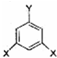 (其中X、Y均不为H),试写出符合上述通式且能发生银镜反应和遇氯化铁溶液发生显色反应的2种物质的结构简式
(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应和遇氯化铁溶液发生显色反应的2种物质的结构简式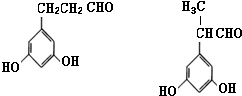 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | B→D→E | CH3-CH2-OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O |
| (2) | 乙炔 | A→C→E | CaC2+2H2O→Ca(OH)2+C2H2↑ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(HCl):碳酸钠溶液 | B. | Cl2(HCl):通过饱和食盐水 | ||
| C. | Na2CO3(NaHCO3):加热固体 | D. | N2(O2):灼热的铜网 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
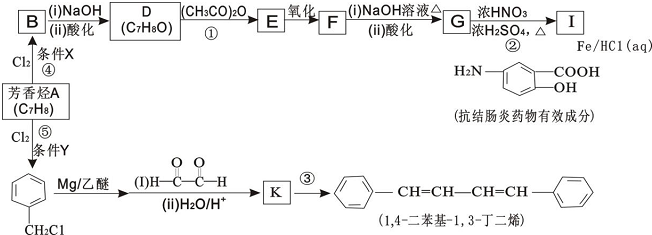
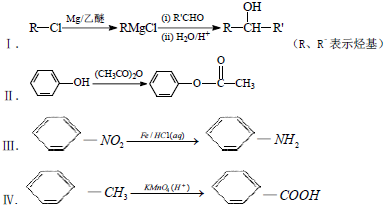
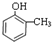
 .
.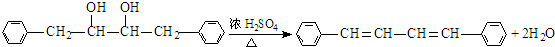 .
.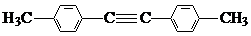 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 序号 | 反应 温度/℃ | c(H2O2)/ mol•L-1 | V(H2O2) /mL | m(MnO2) /g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
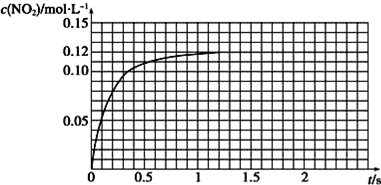
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,可看到有氢气生成 | |
| B. | 将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度NaOH溶液反应,前者速率大于后者 | |
| C. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 | |
| D. | 大理石和盐酸反应制取CO2,增加大理石的用量可加快反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com