
����Ŀ����I�����÷�ӦCuSO4��Fe===Cu��FeSO4�����Ϊԭ��ء�
��1������������________(д����)���缫��ӦΪ__________________________________��
��2�������缫��ӦʽΪ______________________��
��3����Һ��SO42����________���ƶ���
(II)��ҵ�ϳɰ���Ӧ��N2��3H2![]() 2NH3��һ�����ȵĿ��淴Ӧ����Ӧ�����Ǹ��¡���ѹ��������Ҫ���ʵĴ�����
2NH3��һ�����ȵĿ��淴Ӧ����Ӧ�����Ǹ��¡���ѹ��������Ҫ���ʵĴ�����
��4�������1 mol N2��3 mol H2��ϣ�ʹ���ַ�Ӧ���ų���������������ֵ����ԭ����____________________________��
��5��ʵ����ģ�ҵ�ϳɰ�ʱ�����ݻ�Ϊ2 L���ܱ������ڣ���Ӧ����10 min������10 mol NH3������N2��ʾ�Ļ�ѧ��Ӧ����Ϊ________mol��L��1��min��1��
��6��һ�������£����ϳɰ��ķ�Ӧ�ﵽ��ѧƽ��ʱ������˵����ȷ����________��
a������Ӧ���ʺ��淴Ӧ������� b������Ӧ��������淴Ӧ����Ϊ0
c����Ӧ�ﵽ����� d��N2��H2��Ũ�����
e������1 mol N2��ͬʱ������2 mol NH3 f������3 mol H2��ͬʱ������2 mol NH3
���𰸡��� Fe��2e��===Fe2�� Cu2����2e��===Cu �� �÷�Ӧ�ǿ��淴Ӧ��1 mol N2��3 mol H2������ȫ��Ӧ����˷ų�����������С��������ֵ 0.25 acf
��������
��I��(1)�÷�Ӧ�У���ʧ���ӷ���������Ӧ���������������ϵ缫��ӦʽΪ:Fe-2e-�TFe2+��
(2)���������õĽ�����ķǽ�������������ѡͭ������������ͭ���������Һ��������ͭ���ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ:Cu2++2e-�TCu��
(3) ��ԭ����У���Һ��������SO42�����ƶ���
(II)��4���÷�Ӧ�ǿ��淴Ӧ��1 mol N2��3 mol H2������ȫ��Ӧ����˷ų�����������С��������ֵ��
��5��v��NH3��=![]() =
=![]() =0.5mol/��Lmin����
=0.5mol/��Lmin����
v(N2) =![]() v(NH3)������v��N2��=0.25mol/��Lmin����
v(NH3)������v��N2��=0.25mol/��Lmin����
��6��a������Ӧ���ʺ��淴Ӧ������ȣ�˵����Ӧ�ﵽƽ��״̬����ȷ��
b������Ӧ��������淴Ӧ����Ϊ0����ָ��Ӧ��ʼʱ��״̬����Ӧû�дﵽƽ��״̬������
c��N2��ת���ʴﵽ���ֵ��˵����Ӧ�ﵽƽ��״̬����ȷ��
d��N2��H2��Ũ����ȣ���Ӧ��һ���ﵽƽ��״̬������
e��N2��H2��NH3�����������ȣ�����˵���䱣�ֲ��䣬���ж��Ƿ�ﵽƽ��״̬������
f����Ӧ�ﵽ����ȣ�˵����Ӧ�ﵽƽ��״̬����ȷ��
�ʴ�Ϊ��acf��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�Ż��������Ҫ�ɷ���FexS��SΪ-2�������Ⱥ���Fe2+���ֺ���Fe3+����һ�����ĸôŻ�������100mL������ǡ����ȫ��Ӧ��ע����ʯ�������ɷֲ������ᷴӦ��������2��4g���ʣ�0.425mol FeCl2 ��һ����H2S���壬����Һ����Fe3+��������˵����ȷ����
A. ����������ʵ���Ũ��Ϊ4.25mol��L-1
B. �ôŻ�����FexS�У�Fe2+��Fe3+�����ʵ���֮��Ϊ3��1
C. �ɵ�H2S�����ڱ�״���µ����Ϊ2.24L
D. �������FexS��x=0��85
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������½�����A��B���ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g) ![]() 2C(g)+2D(g)����Ӧ���е�10sĩ���ﵽƽ�⣬���A�����ʵ���Ϊ1.8mol��B�����ʵ���Ϊ0.6mol��C�����ʵ���Ϊ0.8mol����
2C(g)+2D(g)����Ӧ���е�10sĩ���ﵽƽ�⣬���A�����ʵ���Ϊ1.8mol��B�����ʵ���Ϊ0.6mol��C�����ʵ���Ϊ0.8mol����
(1)��C��ʾ10s������Ӧ�Ļ�ѧ��Ӧ����Ϊ___________��
(2)��ӦǰA�����ʵ���Ũ����___________��
(3)ƽ��ʱA��ת����Ϊ___________��
(4)��˵���÷�Ӧ�ﵽƽ��״̬����______________��
A.����3molAͬʱ����2molC B.��Ӧ��ϵ�и����ʵİٷֺ�������
C.�������ƽ����Է����������� D.2V��(A)=3V��(C)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2A(g)��B(g)![]() 2C(g)����H����a kJ��mol��1(a>0)����һ���д����Ĺ̶��ݻ��������м���2 mol A��1 mol B����500 ��ʱ��ַ�Ӧ��ƽ���C��Ũ��Ϊ�� mol��L��1���ų�������Ϊb kJ��
2C(g)����H����a kJ��mol��1(a>0)����һ���д����Ĺ̶��ݻ��������м���2 mol A��1 mol B����500 ��ʱ��ַ�Ӧ��ƽ���C��Ũ��Ϊ�� mol��L��1���ų�������Ϊb kJ��
��1����֪��A(g)��X(g)![]() 2B(g)����H����133.2 kJ��mol��1��
2B(g)����H����133.2 kJ��mol��1��
5A(g)��X(g)![]() 4C(g)����H����650.4 kJ��mol��1����a��________��
4C(g)����H����650.4 kJ��mol��1����a��________��
��2����ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�������ʾ���ɴ˿���֪������T1________T2(����>������������<��)��
T/K | T1 | T2 | T3 |
K | 6.86 | 2.45 | 1.88 |
��3����������������Ϊ��ѹ����(��Ӧǰ�����ͬ)����ʼʱ����2 mol A��1 mol B��500 ��ʱ��ַ�Ӧ��ƽ��ų�������Ϊd kJ����d________b(����>������������<��)��
��4����һ���¶��£���һ���ݻ��ɱ�ĺ�ѹ�����У�ͨ��3 mol A��2 mol B��������Ӧ2A(g)��B(g)![]() 2C(g)��ƽ��ʱ�������������ʵ���Ϊ��ʼʱ��80%������ͬһ��Ӧ�¶ȣ�����ͬ�����У�����ʼͶ������Ϊ6 mol A��4 mol B����ƽ��ʱA���������Ϊ________��
2C(g)��ƽ��ʱ�������������ʵ���Ϊ��ʼʱ��80%������ͬһ��Ӧ�¶ȣ�����ͬ�����У�����ʼͶ������Ϊ6 mol A��4 mol B����ƽ��ʱA���������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�������Һ�д����������
A.H+��Ca2+��Cl-��CO32-B.I-��ClO-��K+��H+
C.Na+��Fe3+��SO42-��OH- D.Na+��Cu2+��Cl-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��101 kPaʱ������������ȼ�������Ȼ�������������仯���������й�˵���в���ȷ����(����)
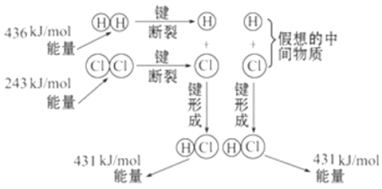
A. 1 mol H2�еĻ�ѧ������ʱ��Ҫ����436 kJ����
B. 2 mol HCl�����еĻ�ѧ���γ�ʱҪ�ͷ�862 kJ����
C. �˷�Ӧ���Ȼ�ѧ����ʽΪ��H2(g)��Cl2(g)==2HCl(g)��H����183 kJ/mol
D. �˷�Ӧ���Ȼ�ѧ����ʽΪ��1/2H2(g)��1/2Cl2(g)==HCl(g)��H����91.5 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������ȡ�Ĵ�ʩ�����û�ѧ��Ӧ���ʽ��͵���
A.��Щʳ��ı�ǩ��ע�������B.�ڸ���������������ӷ�����
C.����̥��Ʒ�м���������̿��D.ȼú����ʱ����ú�۴���ú��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����£�Ksp(AgCl)��1.6��10��10������������ȷ���� ( )
A��AgCl�ڱ���NaCl��Һ�е�Ksp���ڴ�ˮ�е�С
B��AgCl������Һ��c��Cl-��=4��10-5.5mol/L
C����0.001 mol��L��1AgNO3��Һ����0.001 mol��L��1��KCl����������
D����AgCl������Һ�м���NaBr��Һ����ɫ����ת��Ϊ����ɫ��˵��Ksp(AgCl)<Ksp(AgBr)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ����˵����ȷ����
A. �еĽ����Ǵ�����еĽ����ǻ����
B. �еĽ�����磬�еĽ��岻����
C. �����г��õľ������װ���Ǹ��ݽ����ijЩ������Ƶ�
D. ���塢��Һ����Һ�ı����������ܷ���������ЧӦ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com