
分析 A、B、C、D是四种有机物,它们的分子中含有相同的碳原子数,其中A和B是烃,在标准状况下,A对氢气的相对密度是13,则A的相对分子质量是26,结构简式为CH≡CH,B与HCl反应生成C,且B是烃,则B为CH2═CH2,C为CH3CH2Cl,CH3CH2Cl与D混合后加入NaOH并加热,可生成CH2═CH2,氯乙烷在氢氧化钠的醇溶液中发生消去反应生成乙烯,所以D为CH3CH2OH,据此分析解答.
解答 解:A、B、C、D是四种有机物,它们的分子中含有相同的碳原子数,其中A和B是烃,在标准状况下,A对氢气的相对密度是13,则A的相对分子质量是26,结构简式为CH≡CH,B与HCl反应生成C,且B是烃,则B为CH2═CH2,C为CH3CH2Cl,CH3CH2Cl与D混合后加入NaOH并加热,可生成CH2═CH2,氯乙烷在氢氧化钠的醇溶液中发生消去反应生成乙烯,所以D为CH3CH2OH,
(1)通过以上分析知,A、B、C、D为A:CH≡CH、B:CH2═CH2、C:CH3CH2Cl、D:C2H5OH,
故答案为:A:CH≡CH、B:CH2═CH2、C:CH3CH2Cl、D:C2H5OH;
(2)乙烯和HCl在一定条件下发生加成反应生成氯乙烷,反应方程式为CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl,
氯乙烷和NaOH的醇溶液在加热条件下发生消去反应生成乙烯,反应方程式为CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2═CH2+NaCl+H2O,
故答案为:CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl、CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2═CH2+NaCl+H2O.
点评 本题考查有机物推断,为高考高频点,涉及炔、烯烃、氯代烃之间的转化,明确常见物质的官能团及其性质是解本题关键,熟练掌握烷烃、烯烃、醇、卤代烃、醛、羧酸、酯之间的转化及反应条件,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
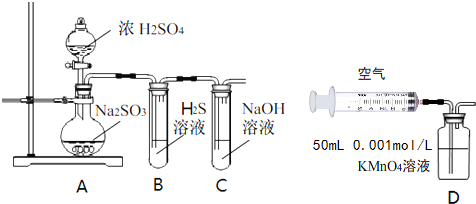
| 实验步骤 | 实验操作 | 预期现象与结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | A的相对分子质量比B的大16 | |
| B. | 该酯分子结构中一定存在双键 | |
| C. | B的相对分子质量比A大14 | |
| D. | 酯、A、B 3种分子中都含有一种相对分子质量大于60的相同基团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
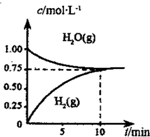 工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,在一定条件下,向体积为1L的密闭容器中充入1mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是( )
工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,在一定条件下,向体积为1L的密闭容器中充入1mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是( )| A. | 达平衡时,CH4(g)的转化率为75% | |
| B. | 0~10min内,v(CO)=0.075mol•L-1•min-1 | |
| C. | 该反应的化学平衡常数K=O.1875 | |
| D. | 当CH4(g)的消耗速率与H2(g)的消耗速率相等时,反应到达平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
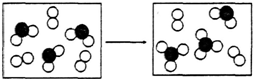 A、B、C、D、E、F是原子序数依次增大的短周期元素,B是短周期中金属性最强的元素,C是地壳中含量最高的金属元素,D单质的晶体是良好的半导体材料,E的最外层电子数与内层电子数之比为3:5,A与E同族.
A、B、C、D、E、F是原子序数依次增大的短周期元素,B是短周期中金属性最强的元素,C是地壳中含量最高的金属元素,D单质的晶体是良好的半导体材料,E的最外层电子数与内层电子数之比为3:5,A与E同族.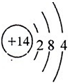
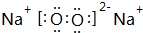 .
. Al(OH)3﹢3H+,生氢氧化铝胶体,能吸附水中悬浮物,使之凝聚达到净水目的
Al(OH)3﹢3H+,生氢氧化铝胶体,能吸附水中悬浮物,使之凝聚达到净水目的查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com