
| A. | CaCl2 和Ca(ClO)2 | B. | Ca(ClO)2 | C. | CaCl2 | D. | CaCO3 |
科目:高中化学 来源: 题型:选择题
| A. | 苯酚显酸性,体现羟基对苯环的影响 | |
| B. | 苯与液溴反应需加催化剂,苯本分与浓溴水混合即可反应,体现苯环对羟基的影响 | |
| C. | 苯的硝化反应只能生成硝基苯,甲苯的硝化反应能生成三硝基甲苯,体现苯环对甲基的影响 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色而甲烷不能,体现苯环对甲基的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱性氧化物 氧化铁 FeO | B. | 酸性氧化物 碳酸气 C0 | ||
| C. | 酸 硫酸 H2S | D. | 盐 纯碱 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
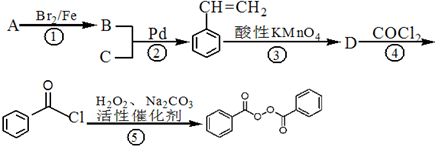
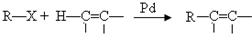
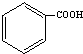 ;
;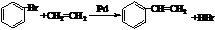 ;
; ),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH
),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH 的流程,无机物任选,注明反应条件.
的流程,无机物任选,注明反应条件.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能/(kJ•mol-1) | 356 | 413 | 336 | 226 | 318 | 452 |
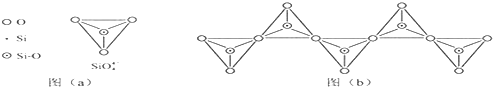
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com