
 .
. ;B与D形成的化合物BD2的结构式是O=C=O,BD2属于共价(填“离子”或“共价”)化合物.
;B与D形成的化合物BD2的结构式是O=C=O,BD2属于共价(填“离子”或“共价”)化合物.分析 有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大.A是所有元素中原子半径最小的元素,故A为H元素;B、C、D同周期且相邻,C的气态氢化物的水溶液显碱性,故C为N元素,则B为C元素,D为O元素;由于原子序数依次增大,而E是同周期元素中金属性最强的元素,故E为Na元素,F的一种氧化物能使品红溶液褪色,即为SO2,故F为S元素.据此分析.
解答 解:有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大.A是所有元素中原子半径最小的元素,故A为H元素;B、C、D同周期且相邻,C的气态氢化物的水溶液显碱性,故C为N元素,则B为C元素,D为O元素;由于原子序数依次增大,而E是同周期元素中金属性最强的元素,故E为Na元素,F的一种氧化物能使品红溶液褪色,即为SO2,故F为S元素.
(1)A为氢元素,C为氮元素,故答案为:氢;氮;
(2)B为碳元素,处于第二周期第IVA族;F为S元素,而S原子的核外有16个电子,核内有16个质子,故S的原子结构示意图为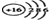 ,
,
故答案为:二;IVA;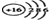 ;
;
(3)E与D形成的化合物E2D2为Na2O2,为离子化合物,由2个钠离子和1个过氧根构成,故电子式为 ;B与D形成的化合物BD2为CO2,C原子和O原子为双键,故结构式为O=C=O,二氧化碳全部由非金属元素构成,故为共价化合物,
;B与D形成的化合物BD2为CO2,C原子和O原子为双键,故结构式为O=C=O,二氧化碳全部由非金属元素构成,故为共价化合物,
故答案为: ;O=C=O;共价;
;O=C=O;共价;
(4)元素的非金属性越强,则最高价含氧酸的酸性越强,由于非金属性Cl>S>C,故酸性HClO4>H2SO4>H2CO3,故答案为:HClO4>H2SO4>H2CO3;
(5)实验室常用KMnO4代替MnO2,与浓盐酸在常温下反应制备G的单质即Cl2,在该反应中同时有MnCl2生成.该反应的离子方程式2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O,故答案为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O.
点评 本题以元素推断为载体,考查核外电子排布式、电子式、半径比较、热化学方程式书写等内容,是对所学知识的综合运用考查,难度不大,注意基础知识的理解掌握.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4甲基4,5二乙基己烷 | B. | 2,3-二甲基-2,4-戊二烯 | ||
| C. | CH3CH(OH)CH2CH3:丁醇 | D. | 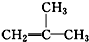 :2-甲基-1-丙烯 :2-甲基-1-丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
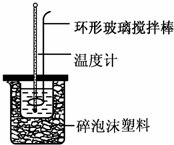 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O(g)=H2O(l)△H=-44kJ/mol,所以该过程是放热反应 | |
| B. | 人类利用的能源都是通过化学反应获得的 | |
| C. | 2CO(g)+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2(g)△H<0,则56gCO和32gO2所具有的总能里大于88g所具有的总能量 | |
| D. | 需要加热的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯乙烯是生产塑料和合成橡胶的重要基本有机原料,乙苯催化脱氢法是目前国内外生产苯乙烯的主要方法,其化学方程式为:
苯乙烯是生产塑料和合成橡胶的重要基本有机原料,乙苯催化脱氢法是目前国内外生产苯乙烯的主要方法,其化学方程式为: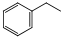 (g)$?_{高温(T)}^{Fe_{2}O_{3}}$
(g)$?_{高温(T)}^{Fe_{2}O_{3}}$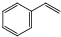 (g)+H2(g)△H=+120kJ•mol-1
(g)+H2(g)△H=+120kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:解答题

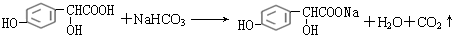 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com