
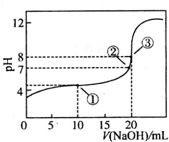
 在25℃时,向50.00mL未知浓度的CH3COOH溶液中逐滴加入0.5mol?L-1的NaOH溶液.滴定过程中,溶液的pH与滴入NaOH溶液体积的关系如右图所示,则下列说法中,不正确的是( )
在25℃时,向50.00mL未知浓度的CH3COOH溶液中逐滴加入0.5mol?L-1的NaOH溶液.滴定过程中,溶液的pH与滴入NaOH溶液体积的关系如右图所示,则下列说法中,不正确的是( )| A、①点所示溶液的导电能力弱于②点 |
| B、图中点③所示溶液中,c(CH3COO-)<c(Na+) |
| C、图中点①所示溶液中水的电离程度大于点③所示溶液中水的电离程度 |
| D、滴定过程中的某点,会有c(Na+)=c(CH3COO-)>c(H+)=c(OH-)的关系存在 |


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
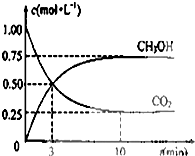 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)查看答案和解析>>
科目:高中化学 来源: 题型:
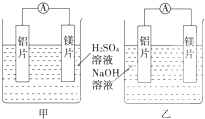 某探究活动小组想利用原电池反应检测金属的活动性顺序,有甲、乙两位同学均使用镁片与铝片作电极,但甲同学将电极放入6mol?L-1稀H2SO4中,乙同学将电极放入6mol?L-1的NaOH溶液中,如图所示.
某探究活动小组想利用原电池反应检测金属的活动性顺序,有甲、乙两位同学均使用镁片与铝片作电极,但甲同学将电极放入6mol?L-1稀H2SO4中,乙同学将电极放入6mol?L-1的NaOH溶液中,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、-131.5kJ?mol-1 |
| B、+352.5kJ?mol-1 |
| C、-352.5kJ?mol-1 |
| D、+131.5kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| B、雾霾天气首要污染物为PM2.5(指大气中直径小于或等于2.5微米的颗粒物),PM2.5在空气中一定形成气溶胶 |
| C、化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础 |
| D、据测定,许多反应的温度每升高10K,其反应速率增加2~4倍.在实验室或工业生产中,常采用加热的方法使化学反应在较高的温度下进行,以提高反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KOH溶液与AlCl3溶液 |
| B、MgCl2溶液与氨水 |
| C、NaAlO2溶液与盐酸 |
| D、Na2CO3溶液与盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:

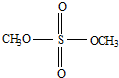 是一种酯类物质,回答下列问题:
是一种酯类物质,回答下列问题: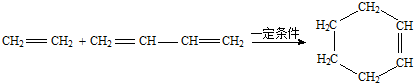 ,Ⅱ有两种同分异构体在一定条件下可相互反应生成
,Ⅱ有两种同分异构体在一定条件下可相互反应生成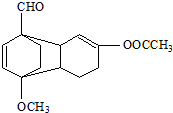 ,这两种同分异构体的结构简式分别为
,这两种同分异构体的结构简式分别为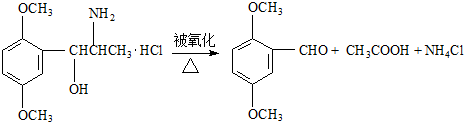
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 所含杂质 | 除去杂质的试剂或方法 | |
| A | KNO3溶液 | KOH | H滴入稀HNO3的同时用pH试纸测定至溶液呈中性 |
| B | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| C | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| D | NaNO3 | CaCO3 | 加稀盐酸溶液、过滤、蒸发、结晶 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14C可用于文物年代的鉴定,是12C的同素异形体 |
| B、向含重金属离子的工业废水中加入明矾,然后再将废水排放 |
| C、利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
| D、配制氯化亚锡(SnCl2)溶液时需加适量盐酸目的是防止其被氧化变浑浊 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com