
将二氧化硫通入溴水中发生如下的反应:SO2+Br2+2H2O═2HBr+H2SO4,反应中转移的电子数和还原剂是( )
|
| A. | 2e﹣,H2SO4 | B. | 4e﹣,SO2 | C. | 2e﹣,Br2 | D. | 2e﹣,SO2 |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
一种盐X和NaOH溶液共热,生成一种有刺激性气味的气体Y,将Y经一系列氧化再溶于水可得一种酸Z,再将Y和Z反应又可生成X,则盐X是( )
A.NH4NO3 B.NH4Cl
C.(NH4)2SO4 D.(NH4)3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质,不用任何试剂即可鉴别的是( )
A.NaCl、NaBr、KI三种无色溶液
B.HCl、NaCl、NaNO3、Na2CO3四种溶液
C.NaBr、HCl、KCl三种溶液
D.淀粉、淀粉碘化钾、碘化钾、溴水四种溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需配制一种仅含五种离子(忽略水电离出的离子)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为5mol/L,下面四个选项中能达到此目的是( )
|
| A. | Na+、K+、SO42﹣、NO3﹣、Cl﹣ | B. | Fe2+、H+、Br﹣、NO3﹣、Cl﹣ |
|
| C. | Ca2+、K+、OH﹣、Cl﹣、NO3﹣ | D. | Al3+、Na+、Cl﹣、SO42﹣、NO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+═Cu2++5Fe2++2S,反应结束后,经处理获得单质硫x mol.下列说法正确的是( )
|
| A. | 反应中硫元素被氧化,所有铁元素均被还原 |
|
| B. | 氧化剂是Fe3+,氧化产物是Cu2+ |
|
| C. | 反应中转移电子的物质的量为xmol |
|
| D. | 反应结束后,测得溶液中三种金属离子的总物质的量为ymol,则原Fe3+的总物质的量为(y﹣x)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
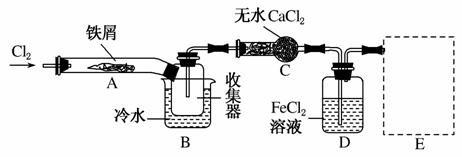
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为________________________ ________________________________________________。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是__________________________。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)________。
(4)装置B中冷水浴的作用为____________________________ __________________;装置C的名称为________;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:________________________________________________________________________。
(5)在虚线框中画出尾气吸收装置E并注明试剂。
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(6)FeCl3与H2S反应的离子方程式为________________________________________________________________________。
(7)电解池中H+在阴极放电产生H2,阳极的电极反应式为________________________________________________________________________。
(8)综合分析实验Ⅱ的两个反应,可知该实验有两个显著优点:
①H2S的原子利用率为100%;
②_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是 ( )
A.钠是电和热的良导体
B.饱和溶液的碱性:NaHCO3大于Na2CO3
C.明矾净水是由于明矾在水中形成Al(OH)3胶体具有吸附作用
D.某溶液焰色反应时,如果火焰呈黄色就说明该溶液一定有钠元素,可能有钾元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com