
��һ�����᳧�������ջ�����(FeS2)����ȡ���ᡣ
����1�����ջ��������Ҫ��ѧ����ʽΪ ���������������������� ��
����2��SO2��O2�ķ�ӦΪ��2SO2��g����O2��g�� 2SO3��g�����÷�Ӧ�����������ܱ������н��У������� ������ţ�����Ϊ��Ӧ�ﵽƽ����ж����ݡ�
2SO3��g�����÷�Ӧ�����������ܱ������н��У������� ������ţ�����Ϊ��Ӧ�ﵽƽ����ж����ݡ�
A��v��(SO2)=v��(SO3)
B������ֵ�����������ٱ仯
C����Ӧ��ϵ���¶Ȳ��ٱ仯
D����������ƽ����Է����������ٱ仯
E�����������ܶȲ��ٱ仯
����3���Ƚ�������ʵ�����Ƚ�����װ�ã���ѧʵ����Ҳ���������Ƚ�����ʵ��ij��ʵ��Ŀ�ġ��Է�������Һ�Ƚ���ʱͨ��ʹ�õ�������________________________����д���ƣ�
����4�����Ṥҵ��������β�����˺���N2��O2�⣬������SO2������SO3�������������ڲⶨ����β����SO2�������Լ���___________________��������ţ�
A.NaOH��Һ����̪��Һ B.KMnO4��Һ��ϡ����
C. ��ˮ����̪��Һ D.��ˮ��������Һ
������ʵ���ҳ������᳧������(��Ҫ�ɷ���Fe2O3������FeS��SiO2)���Ʊ��̷���FeSO4��7H2O����
���вⶨ�̷���Ʒ��FeSO4��7H2O������ʵ�鲽��Ϊ��
a����ȡ5.2 g��Ʒ���ܽ⣬���250 mL��Һ
b����ȡ25.00 ml����Һ����ƿ��
c���������ữ��0. 01 mol/LKMnO4 ��Һ�ζ����յ㣬����KMnO4��Һ���35.00 mL��
�ݴˣ��������
��1���ζ�ʱ��Ӧ�����ӷ���ʽΪ����ɲ���ƽ���ӷ�Ӧ����ʽ����

��2���ζ��ﵽ�յ�ı�־�� ��
��3����Ʒ��FeSO4.7H2O����������Ϊ ��
 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���кϳ��л��߷��ӻ�����ķ�Ӧ�У����ڼӾ۷�Ӧ����(����)


A���٢� B���ۢ�
C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��Ӧ����Ϊ�ɽ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol
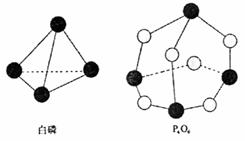 ��ѧ��ʱ�ͷţ������գ�������������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ��mol-1��P-P��198 P-O��360 O=O��498��ӦP4�����ף�+3O2��P4O6�������仯Ϊ( )
��ѧ��ʱ�ͷţ������գ�������������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ��mol-1��P-P��198 P-O��360 O=O��498��ӦP4�����ף�+3O2��P4O6�������仯Ϊ( )
A���ͷ�1638kJ������
B������1638kJ������
C���ͷ�126kJ������
D������126kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��M��G����Ԫ�ط������������ڣ���ԭ��������������X��Zͬ���壬���γ����ӻ�����ZX��Y��Mͬ���壬���γ�MY2��MY3���ַ��ӡ�
��ش��������⣺
�� Y��Ԫ�����ڱ��е�λ��Ϊ________________��
�� ����Ԫ�ص�����������Ӧ��ˮ����������ǿ����_______________��д��ѧʽ�����ǽ�����̬�⻯�ﻹԭ����ǿ����__________________��д��ѧʽ����
�� Y��G�ĵ��ʻ���Ԫ��֮���γɵĻ��������ˮ����������___________��д�������������ʵĻ�ѧʽ����
�� X2M��ȼ���Ȧ�H �� -a kJ��mol-1 ��д��X2Mȼ���ȵ��Ȼ�ѧ����ʽ��
_____________________________________________________________________��
�� ZX�ĵ���ʽΪ___________��ZX��ˮ��Ӧ�ų�����Ļ�ѧ����ʽΪ_______________��
�� ����״̬�£�Z�ĵ��ʺ�FeG2����ɿɳ���أ�װ��ʾ��ͼ���£�����Ӧԭ��Ϊ��
 2Z + FeG2
2Z + FeG2 Fe + 2ZG
Fe + 2ZG
�ŵ�ʱ����ص�������ӦʽΪ_______________________��
���ʱ��_____________��д�������ƣ��缫�ӵ�Դ�ĸ������õ�صĵ����Ϊ___________________��
II. ��ͼ�Ǽ���ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺
(1)��صĸ�����__________(�a����b��)���ü��ĵ缫��Ӧ�ǣ�__________��
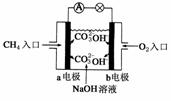
(2)��ع���һ��ʱ���������Һ��pH__________(���������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�����ԣ�HClO��Cl2>Fe3+��SO42���������£����볣����
����K(H2CO3)��K(HClO)��K(HCO3��)��KAl(OH)3��������������ӷ���ʽ��ȷ����
A��0.5mol/L��NaHSO3��Һ��1.0mol/L��NaClO��Һ�������ϣ�
��������HSO3����ClO����SO42����Cl����H��
B��С�մ���Һ��ƫ��������Һ��ϣ�HCO3����AlO2����H2O��Al(OH)3��+CO32��
C����84������Һ����Ҫ�ɷ�ΪNaClO��¶���ڿ����б��ʣ�
����2ClO����CO2��H2O��CO32����2HClO
D���ڡ�84������Һ�еμ�FeSO4��Һ��2Fe2����ClO����H2O��2Fe3����Cl����2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ�е�������ǿ����
A��5L 0.1 mol ��L��1NH3��H2O �� B��5L mol ��L��1 ����
C��0.1L 0.1 mol ��L��1H3PO4��Һ �� D��0.1L 0.1 mol ��L��1 Ba(OH)2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ӦA(g)+3B(g) 2C(g)+2D(g)�ڲ�ͬ����²�÷�Ӧ���ʣ����з�Ӧ����������
2C(g)+2D(g)�ڲ�ͬ����²�÷�Ӧ���ʣ����з�Ӧ����������
A����(A)=0.1 mol ��L��1��s��1 B����(B)=0.6 mol ��L��1��s��1
C����(C)=0.5 mol ��L��1��s��1 D����(D)=0.4 mol ��L��1��s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
I����֪һ����̼��ˮ�����ķ�ӦΪ��CO��g����H2O��g�� CO2��g����H2��g��
CO2��g����H2��g��
��1��T��ʱ����һ������������У�ͨ��һ������CO��g����H2O��g����������Ӧ�������¶Ȳ��䣬������Ũ����ʱ��仯���±�������
T��ʱ���ʵ�Ũ�ȣ�mol•L-1���仯
| ʱ��/ min | CO | H2O��g�� | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
��5��6minʱ�������DZ����¶Ⱥ��������ʱ���ı�ijһ�������õġ���4��5min֮�䣬�ı������������������ ���� ��T��ʱ�û�ѧ��Ӧ��ƽ�ⳣ������������������ ��
�ڸ��¶��£�����һ�ݻ��̶����ܱ�������ͬʱ����1.0 mol CO��3.0 mol H2O��1.0 mol CO2��2.0mol H2����Ӧ������������ ���С��������Ӧ�����淴Ӧ����
��2����֪420��ʱ���û�ѧ��Ӧ��ƽ�ⳣ��Ϊ9�������Ӧ��ʼʱ��CO��H2O��g����Ũ�ȶ���0.01 mol•L-1����CO�ڴ������µ�ת����Ϊ�������������� ��������������������ܱ��������ٳ���1 mol�����ƽ��ʱCO��ת���� ���������䡱����С����
��3��397��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ12�����жϸ÷�Ӧ�ġ�H�������� 0���>��������������<������
II����ҵ�Ͽ���CO��H2��һ�������ºϳɼ״�����ӦΪ��
CO��g��+2H2��g��⇌ CH3OH��g����H��Q kJ•mol-1
�����ݻ���Ϊ2L��a��b��c��d��e����ܱ������зֱ����1mol CO��2mol H2�Ļ�����壬���£�����ʵ�飬��������������ͼ1��ͼ2��
 |
��1���÷�Ӧ��Q 0��ѡ���������������=������ͬ����K1 K2��
��2��300��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ ��
��3��������d�е�ƽ��״̬ת�䵽����c�е�ƽ��״̬���ɲ�ȡ�Ĵ�ʩ�У�____________
(���ٴ�2��) ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������100 mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼����(�ۼ�ֵ�����������Ϊ������)��
| ʱ��(min) | 1 | 2 | 3 | 4 | 5 |
| �������(mL) | 50 | 120 | 232 | 290 | 310 |
(1)��һʱ���(ָ0��1��1��2��2��3��3��4��4��5 min)��Ӧ�������___________��
ԭ���� ��
(2)��2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����(����Һ�������)
(3)�����Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ����������������������зֱ�������
����������Һ������Ϊ���е���__________��
A������ˮ B��NaCl��Һ C��NaNO3��Һ D��CuSO4��Һ E��Na2CO3��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com