
| A、CO2 能使漂白粉水溶液先变浑浊后变澄清,SO2 也有同样现象 |
| B、加热条件下,Na与O2 反应生成Na2O2,Li与O2反应也声称Li2O2 |
| C、常温下,浓硝酸能使铁、铝钝化,浓硫酸也能使铁、铝钝化 |
| D、氯气可置换出KI溶液中的碘,氟气也可置换出KI溶液中的碘 |


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强酸性溶液中:Na+,Fe2+,Cl-,ClO- |
| B、加入Al能放出的H2溶液中:Cl-,HCO3-,NO3-,NH4+ |
| C、在由水电离出的c(OH-)=10-13mol?L-1的溶液中:Fe2+,Al3+,NO3-,Cl- |
| D、pH=11的溶液中:CO32-,Na+,[Al(OH)4]-,NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
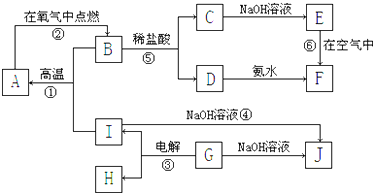
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、白色污染是指橡胶造成的污染 |
| B、硫和氮的氧化物是形成酸雨的主要物质 |
| C、汽车尾气的排放是造成温室效应的主要原因 |
| D、含磷洗涤剂的使用时造成水体富营养化的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:
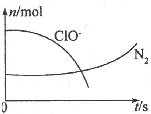 某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中N2、ClO-的物质的量随时间变化的曲线如右图所示.下列判断不正确的是( )
某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中N2、ClO-的物质的量随时间变化的曲线如右图所示.下列判断不正确的是( )| A、该反应的氧化剂是ClO- |
| B、消耗1 mol还原剂,转移3 mol电子 |
| C、氧化剂与还原剂的物质的量之比为2:3 |
| D、反应后溶液的酸性明显增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,l mol N2与足量H2反应生成NH3,转移电子6NA |
| B、标准状况下,11.2 L CCl4中含有C-Cl键的数目为2NA |
| C、1 mol甲基(-14C1H3)含有的中子数和电子数分别为8NA、9NA |
| D、1 mol?L-1Na2CO3溶液中含有的钠离子总数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com