
现有含MgCl2、AlCl3均为n mol的混合溶液,向其中滴NaOH溶液至过量。加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是(离子形成沉淀或沉淀的溶解与溶液pH的关系如下表) ( )。
| 离子 | Mg2+ | Al3+ | 物质 | Al(OH)3 |
| 开始沉淀时的pH | 8.93 | 3.56 | 开始溶解时的pH | 8.04 |
| 完全沉淀时的pH | 10.92 | 4.89 | 完全溶解时的pH | 12.04 |

科目:高中化学 来源: 题型:
有机物A、B、C、D、E都是常见的有机物,能发生如图所示的转化,已知A的分子式为C10H20O2,则符合此转化关系的A的可能结构有( )
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
美国宇航局“凤凰”号火星登陆器的显微、电子化学及传导分析仪对两份土壤样本的分析发现,火星北极区表层土壤可能含有高氯酸盐,可创造不利于任何潜在生命的恶劣环境。则下列说法错误的是 ( )。
A.含有高氯酸盐的土壤不利于生命存在与高氯酸盐具有较强的氧化性有关
B.当元素处于最高价态时一定具有强氧化性
C.可以考虑用加入亚铁盐等还原性物质的方法改善这种土壤
D.一定条件下高氯酸盐能与浓盐酸反应生成氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列Ⅰ、Ⅱ因果描述正确且二者有必然联系的是 ( )。
| Ⅰ(原因) | Ⅱ(结果) | |
| A | 木炭呈黑色 | 木炭常用作能源 |
| B | 一氧化碳具有还原性 | 工业上用一氧化碳冶炼金属 |
| C | 碳酸钠属于碱类 | 用热的纯碱溶液清洗油污器具 |
| D | 二氧化碳是酸性氧化物 | 二氧化碳能与水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
硅及其化合物对人类现代文明具有特殊贡献。请回答下列有关问题:
(1)硅原子的结构示意图为:________。
(2)下列物品或设备所用材料属于硅酸盐的是____________________________ _______________________________________。
①长江三峡水泥大坝 ②光导纤维 ③陶瓷坩埚
④普通玻璃 ⑤硅太阳能电池
A.①②③ B.③④⑤
C.②③④ D.①③④
(3)下列说法正确的是________。
A.在粗硅的制取中发生2C+SiO2 2CO↑+Si,硅被还原,所以碳的还原性大于硅的还原性
2CO↑+Si,硅被还原,所以碳的还原性大于硅的还原性
B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中
C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2
D.由Na2CO3+SiO2 CO2↑+Na2SiO3可知硅酸的酸性大于碳酸
CO2↑+Na2SiO3可知硅酸的酸性大于碳酸
(4)常温下,SiCl4为液态,沸点为57.6 ℃,在空气中冒白雾。制备高纯度硅的中间产物SiCl4中溶有液态杂质,若要得到高纯度SiCl4,应采用的方法是____________;用化学方程式及必要的文字解释SiCl4在空气中冒白雾的原因:______________________________________________________________
_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150 mL 4 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24 L NO(标准状况下),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为 ( )。
A.0.21 mol B.0.25 mol
C.0.3 mol D.0.35 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属的冶炼方法叙述不正确的是 ( )。
| 金属 | 存在形式 | 冶炼方法 | |
| A | 金 | 游离态 | 金子比沙子密度大,利用水洗法直接分离 |
| B | 银 | 化合态 | 银的金属性弱,用加热Ag2O的方法冶炼 |
| C | 铁 | 化合态 | 铝的金属性比铁强,可用铝热法炼铁 |
| D | 钠 | 化合态 | 钠的金属性强,一般还原剂很难将其还原出来,所以用电解饱和NaCl溶液的方法冶炼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物是中学化学中的一类重要物质,下列关于铁元素的叙述中正确的是 ( )。
A.2Fe3++Fe===3Fe2+成立说明氧化性:Fe3+>Fe2+
B.25 ℃,pH=0的溶液中,Al3+、NH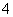 、NO
、NO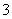 、Fe2+可以大量共存
、Fe2+可以大量共存
C.5.6 g铁与足量的氯气反应失去电子为0.2 mol
D.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+===Fe3++4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
向某FeBr2溶液中通入1.12 L(标准状况)的Cl2,测得溶液中c(Br-)=3c(Cl-)=0.3 mol·L-1。反应过程中溶液的体积变化不计。则下列说法中正确的是 ( )。
A.原溶液的浓度为0.1 mol·L-1
B.反应后溶液中c(Fe3+)=0.1 mol·L-1
C.反应后溶液中c(Fe3+)=c(Fe2+)
D.原溶液中c(Br-)=0.4 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com