
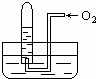
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
|
| A. | 2.1mL | B. | 2.4mL | C. | 3.6mL | D. | 4mL |
考点:
化学方程式的有关计算.
分析:
可能发生的反应为:4NO2+O2+2H2O=4HNO3,3NO2+H2O=2HNO3+NO,试管中O2和NO2气体按体积比1:4混合全部溶解,液体充满试管,假定全部为二氧化氮,剩余气体体积为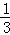 ×12mL=4mL,实际是结果剩余2mL气体,小于4mL,则说明剩余气体为NO或氧气,
×12mL=4mL,实际是结果剩余2mL气体,小于4mL,则说明剩余气体为NO或氧气,
若为氧气,根据4NO2+O2+2H2O=4HNO3,求出参加此反应的O2,最后相加得到原来的氧气;
若为NO,先根据3NO2+H2O=2HNO3+2NO求出过量的NO2,然后根据4NO2+O2+2H2O=4HNO3求出参加此反应的NO2,据此解答.
解答:
解:可能发生的反应为:4NO2+O2+2H2O=4HNO3,3NO2+H2O=2HNO3+NO,试管中O2和NO2气体按体积比1:4混合全部溶解,液体充满试管,假定全部为二氧化氮,剩余气体体积为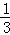 ×12mL=4mL,实际是结果剩余2mL气体,小于4mL,则说明剩余气体为NO或氧气,
×12mL=4mL,实际是结果剩余2mL气体,小于4mL,则说明剩余气体为NO或氧气,
若为氧气,则参加反应的气体为12mL﹣2mL=10mL,根据4NO2+O2+2H2O=4HNO3,可知参加此反应的NO2的体积为10mL×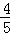 =8mL,参加反应的O2的体积为10mL﹣8mL=2mL,原混合气体中O2的体积为2mL+2mL=4mL;
=8mL,参加反应的O2的体积为10mL﹣8mL=2mL,原混合气体中O2的体积为2mL+2mL=4mL;
若剩余气体为NO气体,根据3NO2+H2O=2HNO3+NO,可知过量的NO2为3×2mL=6mL,反应4NO2+O2+2H2O=4HNO3消耗的气体总体积为12mL﹣6mL=6mL,则反应消耗的氧气为6mL×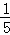 =1.2mL,即原混合气体中O2的体积为1.2mL;
=1.2mL,即原混合气体中O2的体积为1.2mL;
故选D.
点评:
本题考查了氮氧化物的性质、混合物有关计算,难度中等,关键是分析剩余气体的成分.


科目:高中化学 来源: 题型:
下列关于油脂的说法中,不正确的是( )
A.油脂水解后的产物经氧化为人体提供热能
B.油脂能溶解维生素A、D、E、K
C.油脂能储备热能
D.多吃动物脂肪比多吃植物油好
查看答案和解析>>
科目:高中化学 来源: 题型:
用0.1 mol·L-1的Na2SO3溶液30 mL恰好将2×10-3mol的XO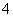 还原,则元素X在还原产物中的化合价是( )
还原,则元素X在还原产物中的化合价是( )
A.+1 B.+2 C.+3 D.+4
查看答案和解析>>
科目:高中化学 来源: 题型:
(1) (8分)某无色溶液含下列8种离子中某几种:Na+、H+、Mg2+、Ag+、Cl-、OH-、
HCO3-、NO3-。已知该溶液可与Al2O3反应,则:
① 若溶液与Al2O3反应,有Al3+生成,则溶液一定有________,一定不含有________。
② 若溶液与 Al2O3反应,有AlO2-生成,则溶液一定有________,可能含有________。
(2)(5分)有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,
用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无反应现象。
由此,可判定各试剂瓶中所盛试剂为:
A________,B________,C________,D________,E________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组元素中按微粒半径递增顺序排列的是( )
|
| A. | Li K Na | B. | Ba2+ Ca2+ Mg2+ |
|
| C. | Ca2+ K+ Cl﹣ | D. | N O F |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列热化学方程式:
①H2(g)+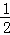 O2(g)═H2O(g)△H1=a kJ•mol﹣1②2H2(g)+O2(g)═2H2O(g)△H2=b kJ•mol﹣1
O2(g)═H2O(g)△H1=a kJ•mol﹣1②2H2(g)+O2(g)═2H2O(g)△H2=b kJ•mol﹣1
③H2(g)+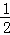 O2(g)═H2O(l)△H3=c kJ•mol﹣1④2H2(g)+O2(g)═2H2O(l)△H4=d kJ•mol﹣1
O2(g)═H2O(l)△H3=c kJ•mol﹣1④2H2(g)+O2(g)═2H2O(l)△H4=d kJ•mol﹣1
下列关系式中正确的是( )
|
| A. | a<c<0 | B. | b>d>0 | C. | 2a=b<0 | D. | 2c=d>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
5.7g汽油[主要成分是辛烷(C8H18),平均相对分子质量为114]完全燃烧生成液态水和CO2放出275.9kJ的热量,汽油的燃烧热△H= .
由于石油资源有限,且汽油燃烧会产生严重的污染,未来应该会用氢气作为燃料来取代汽油,生产新型环保汽车.已知:2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol,H2O(l)═H2O(g)△H=+44kJ/mol.
(1)写出氢气和氧气反应生成液态水的热化学方程式
(2)常温下,若要得到857.4kJ的热量,需氢气的质量为 克.
查看答案和解析>>
科目:高中化学 来源: 题型:
德国化学家凯库勒认为,苯分子的结构中碳碳间以单、双键交替排列结合成环状.为了验证凯库勒的观点,某学生设计了以下实验方案:
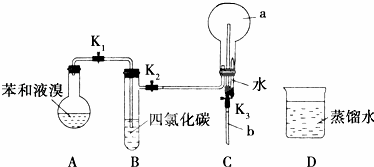
①按如图所示的装置连接好仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2、K3止水夹;
④待烧瓶C中收集满气体后,将导管b的下端插入烧杯D里的水中,挤压预先盛有水的胶头滴管,观察实验现象.
(1)A中所发生反应的反应类型为 ,能证明凯库勒观点错误的实验现象是 .
(2)装置B的作用是 .
(3)烧瓶C的容积为500mL,收集气体时,由于空气未排尽,最终水未能充满烧瓶,假设烧瓶中混合气体对氢气的相对密度为37.9,则实验结束后,进入烧杯中的水的体积为 mL(空气的相对分子质量以29计算).
查看答案和解析>>
科目:高中化学 来源: 题型:
某苯的衍生物,含有两个互为对位的取代基,其分子式为C8H10O,其中不跟NaOH溶液反应的衍生物种类有()
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com