
用软锰矿(主要成分为MnO2)生产高锰酸钾产生的锰泥中,还含有18%的MnO2、3%的KOH(均为质量分数),及少量Cu、Pb的化合物等,用锰泥可回收制取MnCO3,过程如图:
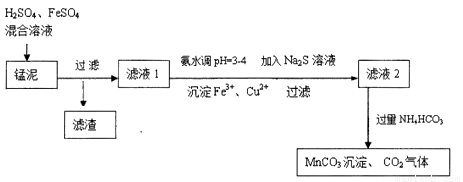
(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强。通常用来酸化高锰酸钾的酸是
(2)除去滤液1中Cu2+的离子方程式是
(3)经实验证明:MnO2稍过量时,起始H2SO4、FeSO4混合溶液中c(H+)/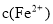 <0.7时,滤液1中能够检验出有Fe
<0.7时,滤液1中能够检验出有Fe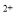 ;
;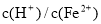 ≥0.7时,滤液1中不能检验出有Fe2+。根据上述信息回答①②③:
≥0.7时,滤液1中不能检验出有Fe2+。根据上述信息回答①②③:
①检验Fe2+是否氧化完全的实验操作是__________。
②生产时H2SO4、FeSO4混合溶液中c(H+)/c(Fe2+)控制在0.7~1之间,不宜过大,请从节约药品的角度分析,原因是__________。
③若c(H+)/c(Fe2+)>1,调节c(H+)/c(Fe2+)到0.7~1的最理想试剂是_(填序号)
a.NaOH溶液 B.铁粉 c.MnO。
(4)写出滤液2中加入过量NH4HCO3反应的离子方程式__________。
(5)上述过程锰回收率可达95%,若处理1740 kg的锰泥,可生产MnCO3__________kg。
 每课必练系列答案
每课必练系列答案科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
某芳香烃的分子式为C10H14,不能使溴水褪色,但可使酸性高锰酸钾溶液褪色,分子结构中只含有一个侧链烃基,则此侧链烃基的结构共有()
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
用纤维素为主要原料制备乙酸乙酯的路线如下:
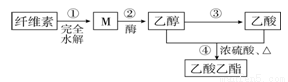
下列说法正确的是
A.若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯
B.M虽然分子结构中无醛基,但仍然可以发生银镜反应
C.步骤②,1molM完全反应可以生成3mol乙醇
D.③和④都发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2016届河南省原推荐高三四月高考仿真模拟理综化学试卷(解析版) 题型:实验题
青蒿素,是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工艺为:
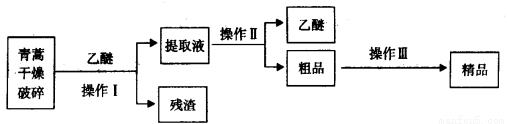
请回答下列问题:
(1)对青蒿进行干燥破碎的目的是_____________。
(2)操作I需要的玻璃仪器主要有:烧杯、___________,为加速操作I的进行,最好采用________________的方法,操作Ⅱ的名称是___________________。
(3)操作Ⅲ的主要过程可能是_____________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
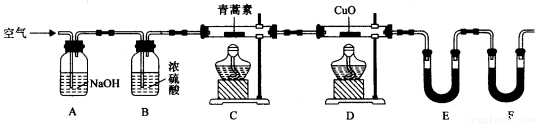
①装置E中盛放的物质是______________,装置F中盛放的物质是________________。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是_______________。
③用合理改进后的装置进行试验,称得:

则测得青蒿素的最简式是__________________。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与____________(填字母)具有相同的性质。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响, 其结果如下图所示:
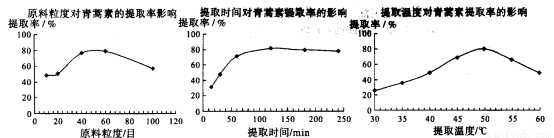
由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为_______________。
A.80目、100分钟、50℃ B.60目、120分钟、50℃ C.60目、120分钟、55℃
查看答案和解析>>
科目:高中化学 来源:2016届河南省原推荐高三四月高考仿真模拟理综化学试卷(解析版) 题型:选择题
化学与生活、社会发展息息相关,下列有关说法正确的是
A.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
B.“丹砂(HgS)烧之成水银,积变又还成了丹砂”,该过程发生了分解、化合、氧化还原反应
C.干燥剂硅胶和硅橡胶的主要化学成分都是二氧化硅
D.铜制品在潮湿的空气中生锈,其主要原因是发生了析氢腐蚀
查看答案和解析>>
科目:高中化学 来源:2016届广东省佛山市高三4月二模理综化学试卷(解析版) 题型:选择题
利用电导率传感器可绘制电导率曲线图,下图为用0.1mol/LNaOH溶液滴定10mL0.lmol/L盐酸过程中的电导率曲线。下列说法错误的是
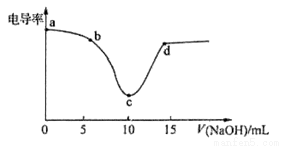
A.电导率传感器能用于判断酸碱中和滴定的终点
B.该过程中,a点所示溶液的导电性最强
C.c点电导率最小是因为此时溶液中导电微粒数目最少
D.d点所示溶液中存在:c(Cl一)+c(OH一)=c(H+)+c(Na+)
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高考模拟理综化学试卷(解析版) 题型:推断题
以煤为原料可合成涂料H(如下图)。B分子式为C2H6O,能与钠反应放出氢气。(注:流程中某些反应条件没有给出)。


请回答:
(1)流程中煤的综合利用的工艺名称为 。
(2)B的结构简式是 ,E中含氧官能团的名称是 。
(3)G→H反应的化学方程式 。
(4)对于化合物F,下列说法正确的是 。
A、能发生银镜反应 B、能使Br2的CCl4溶液褪色
C、能发生水解反应 D、能与金属钠反应
(5)下列有机物与G不是互为同分异构体的是 。

(6)从 →E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式) 。
→E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式) 。
查看答案和解析>>
科目:高中化学 来源:2016届天津市高三下学期八校联考化学试卷(解析版) 题型:选择题
生活中碰到的某些问题常常涉及到化学知识,下列分析正确的是
A.碳酸氢钠可用于制备纯碱、治疗胃酸过多的药剂
B.胃酸过多的人不宜吃海带、鸡肉、苹果等酸性食物
C.人造纤维、合成纤维和光导纤维都是有机高分子化合物
D.1mol葡萄糖能水解成2mol乙醇和2mol二氧化碳
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二下期中化学试卷(解析版) 题型:选择题
下列实验操作不能达到预期目的的是
实验目的 | 操作 | |
A | 欲比较水和乙醇中羟基氢的活泼性 | 用金属钠分别与水和乙醇反应 |
B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴加酸性KMnO4溶液,看紫红色是否褪去 |
C | 欲确定磷、砷两元素非金属性的强弱 | 测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
D | 欲除去苯中混有的苯酚 | 向混合液中加入NaOH溶液,充分反应后,分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com