
能正确解释下列反应原理的离子方程式是 ( )
A.用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+
B.用小苏打治疗胃酸过多:CO2-3+2H+=CO2↑+H2O
C.用氯化铁溶液腐蚀印刷线路板上的铜:Fe3++ Cu=Fe2++ Cu2+
D.用碳酸钠溶液浸泡锅炉水垢:CaSO4+CO2-3=CaCO3↓+SO2-4
科目:高中化学 来源: 题型:
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列事实解释正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
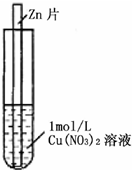 (2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.
(2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁 | ||
| B、饱和FeCl3溶液在20℃时呈现棕黄色,100℃呈现红褐色,不能用平衡移动原理来解释 | ||
C、在
| ||
| D、在原电池装置中,电子从负极流出,沿导线流入正极,经溶液或盐桥回到负极 |
查看答案和解析>>
科目:高中化学 来源:浙江省模拟题 题型:单选题
| 下列现象或反应的原理解释正确的是 | |||||||||||||||
|
[ ] | |||||||||||||||
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com