
 NH3和CO2是两种重要的化工原料.
NH3和CO2是两种重要的化工原料.分析 (1)反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断;
(2)结合热化学方程式和盖斯定律计算得到热化学方程式,依据热化学方程式定量关系计算;
(3)①在300℃、新型催化剂的作用下,一氧化碳与氢气反应生成甲烷和水;
②根据化学平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积列平衡常数的表达式,温度越高甲烷物质的量越小,说明升温平衡逆向进行;
升高温度平衡甲烷的变化判断平衡常数的变化;
反应速率之比等于化学方程式计量数之比,化学反应速率是υ(H2)=4υ(CH4)计算,
500℃时,若将处于平衡状态的反应容器体积增加到2V L,压强减小,平衡向气体体积增大的方向进行,
解答 解:(1)N2+3H2?2NH3.反应是气体体积减小的放热反应,
a.反应速率之比等于化学方程式计量数之比为正反应速率,2v(H2)正=3v(NH3)逆,说明氨气正逆反应速率相同,反应达到平衡状态,3v(H2)正=2v(NH3)逆 ,不能说明正逆反应速率相同,故a错误;
b.单位时间生成mmolN2的同时消耗3mmolH2 ,能说明氢气正逆反应速率相同反应达到平衡状态,故b正确;
c.反应前后气体质量不变,体积不变,混合气体的密度不再随时间变化,不能说明反应达到平衡状态,故c错误;
d.$\frac{c({N}_{2})•{c}^{3}({H}_{2})}{{c}^{2}(N{H}_{3})}$为该反应的平衡常数的倒数,平衡常数随温度变化,$\frac{c({N}_{2})•{c}^{3}({H}_{2})}{{c}^{2}(N{H}_{3})}$不再随时间变化说明反应达到平衡状态,故d正确;
故答案为:bd;
(2)CO2和NH3可用于合成尿素[CO(NH2)2],反应原理如下::
①CO2(g)+2NH3(g)=H2NCOONH4(s),△H=-159.47kJ/mol
②H2NCOONH4(s)=CO(NH2)2(s)+H2O(l)△H=+28.49kJ/mol,
盖斯定律计算①+②得到:CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)△H=-130.98KJ/mol
若总反应放热261.96kJ,则反应的CO2=$\frac{261.96KJ}{130.98KJ}$×1mol=2mol,
故答案为:2;
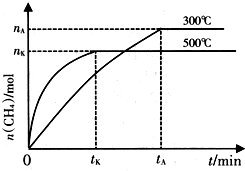
(3)新型催化剂,将CO2转变为甲烷.在1.01×l05Pa、300℃条件下,CO2与H2以1:4体积比发生该反应,
①在300℃、新型催化剂的作用下,一氧化碳与氢气反应生成甲烷和水,方程式为:CO2+4H2$?_{新型催化剂}^{300℃}$CH4+2H2O,
故答案为:CO2+4H2$?_{新型催化剂}^{300℃}$CH4+2H2O;
②化学平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,CO2+4H2$?_{新型催化剂}^{300℃}$CH4+2H2O;反应物和生成物都是气体,平衡常数表达式为K=$\frac{c(C{H}_{4}){c}^{2}({H}_{2}O)}{c(C{O}_{2}){c}^{4}({H}_{2})}$,
由图象可知升高温度甲烷的物质的量减少,平衡向逆反应方向移动,K减小,正反应为放热反应,
υ(H2)=4υ(CH4)=$\frac{\frac{4{n}_{A}}{V}}{{t}_{A}}$=$\frac{4{n}_{A}}{V{t}_{A}}$,
CO2+4H2$?_{新型催化剂}^{300℃}$CH4+2H2O,反应容器体积增大,压强减小,化学平衡向气体体积增大的方向进行,逆反应是气体体积增大的反应,
故答案为:$\frac{c(C{H}_{4}){c}^{2}({H}_{2}O)}{c(C{O}_{2}){c}^{4}({H}_{2})}$;放热反应;$\frac{4{n}_{A}}{V{t}_{A}}$mol/(L•min);逆反应;反应容器体积增大,压强减小,化学平衡向气体体积增大的方向进行,逆反应是气体体积增大的反应.
点评 本题考查化学平衡的影响因素、化学平衡的标志、盖斯定律的应用及平衡常数计算等问题,难度中等.侧重考查学生分析和解决问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | SO2、O2、SO3中 | B. | SO3中 | C. | SO2、O2中 | D. | SO2、SO3中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用食品添加剂与提倡绿色食品相违背 | |
| B. | 含有食品添加剂的食品应该少食,以防中毒 | |
| C. | 没有加任何添加剂的天然食品是最安全的 | |
| D. | 食品添加剂在合理限量范围内不影响人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应达到平衡后,其他条件不变,只改变压强,平衡不移动 | |
| B. | 上述反应过程中的平均相对分子质量增大 | |
| C. | 单位时间内反应物浓度的减少等于生成物浓度的增加 | |
| D. | 若在前10s内B减少了xmol,则在前20s内A减少小于2xmol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

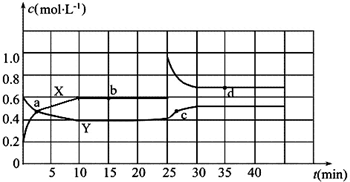
| A. | 该反应的△H>0 | B. | 达平衡时,3v(H2)正=v(CO2)逆 | ||
| C. | a点对应的H2的平衡转化率为90% | D. | b点对应的平衡常数K值大于c点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com