
【题目】I.某同学用下图所示的装置做了有关氨气的性质实验。
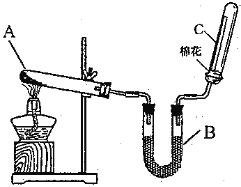
(1)写出A处氯化铵固体与熟石灰共热反应的化学方程式:_____________________________。
(2)B中盛放的是碱石灰,其作用是_____________________________。
(3)氨气极易溶于水,在氨水中滴加酚酞,现象是_________________________________。
(4)检验氨气的方法是___________________________________________________________。
Ⅱ.乙烯是一种重要的有机化工原料。在一定条件下乙烯可发生如下转化:
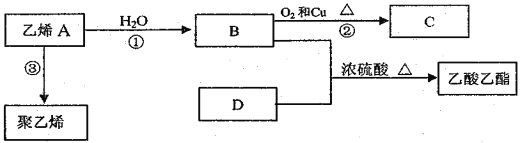
(1)乙烯的结构简式是_______________,D的分子式是_______________。
(2)B中含氧官能团的名称是_____________,③的反应类型是______________。
(3)写出反应②的化学方程式: ________________________________________。
【答案】 2NH4Cl + Ca(OH)2 ![]() CaCl2+ 2NH3↑+2H2O 干燥氨气 溶液变红 湿润的红色石蕊试纸靠近收集试管口,若试纸变蓝,则证明是氨气。或蘸有浓盐酸的玻璃棒靠近收集试管口,若产生白烟,则证明是氨气 CH2=CH2 C2H4O2 羟基 加聚反应
CaCl2+ 2NH3↑+2H2O 干燥氨气 溶液变红 湿润的红色石蕊试纸靠近收集试管口,若试纸变蓝,则证明是氨气。或蘸有浓盐酸的玻璃棒靠近收集试管口,若产生白烟,则证明是氨气 CH2=CH2 C2H4O2 羟基 加聚反应 ![]()
【解析】分析:I.考查氨气的实验室制备、实验现象的描述和氨气的检验。
II.考查有机推断、有机物结构简式和分子式的书写、有机反应类型的判断、有机方程式的书写。反应①为CH2=CH2与H2O发生加成反应,B为CH3CH2OH;反应②为CH3CH2OH的催化氧化反应,C为CH3CHO;B(CH3CH2OH)与D反应生成乙酸乙酯,D为CH3COOH。
详解:I.(1)NH4Cl与熟石灰共热生成CaCl2、NH3和H2O,反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
(2)A中制得的NH3中混有H2O(g),B中盛放的是碱石灰,碱石灰能吸收H2O(g),不吸收NH3,其作用是干燥NH3。
(3)NH3极易溶于水,NH3溶于水发生反应NH3+H2O![]() NH3·H2O,NH3·H2O属于弱碱,NH3·H2O的电离方程式为NH3·H2O
NH3·H2O,NH3·H2O属于弱碱,NH3·H2O的电离方程式为NH3·H2O![]() NH4++OH-,氨水呈碱性,在氨水中滴加酚酞,现象是:溶液变红。
NH4++OH-,氨水呈碱性,在氨水中滴加酚酞,现象是:溶液变红。
(4)检验氨气的方法是:湿润的红色石蕊试纸靠近收集试管口,若试纸变蓝,则证明是氨气。或蘸有浓盐酸的玻璃棒靠近收集试管口,若产生白烟,则证明是氨气。
II.反应①为CH2=CH2与H2O发生加成反应,B为CH3CH2OH;反应②为CH3CH2OH的催化氧化反应,C为CH3CHO;反应③为CH2=CH2的加聚反应;B(CH3CH2OH)与D反应生成乙酸乙酯,D为CH3COOH。
(1)乙烯的结构简式为CH2=CH2。D为CH3COOH,其分子式为C2H4O2。
(2)B为CH3CH2OH,其中含氧官能团的名称是羟基。反应③为CH2=CH2发生加聚反应生成聚乙烯,反应类型为加聚反应。
(3)反应②为CH3CH2OH催化氧化成CH3CHO,反应的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


科目:高中化学 来源: 题型:
【题目】重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.氘(D)原子核外有 1 个电子
B.1H与 D 互为同位素
C.H2O 与 D2O 互为同素异形体
D.1H218O与D216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料﹣﹣﹣﹣﹣铁红(Fe2O3),
具体生产流程如图:![]()
试回答下列问题:
(1)“酸溶”过程中Fe3O4发生反应的离子反应方程式为;
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有、玻璃棒和烧杯等;步骤Ⅳ中应选用试剂调节溶液的pH(填字母编号)
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是;
(4)步骤Ⅴ的反应温度一般需控制在35℃以下,其目的是;
(5)步骤Ⅵ中发生反应的化学反应方程式为;
(6)步骤Ⅴ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为8.5,c(Fe2+)=1×10﹣6 molL﹣1 . 试判断所得的FeCO3中是否含有Fe(OH)2(填“是”或“否”),请通过简单计算说明理由(已知:Ksp[Fe(OH)2]=4.9×10﹣17).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表示正确的是( )
A.乙酸的结构简式:C2H4O2
B.乙烯的电子式: ![]()
C.硫离子结构示意图: ![]()
D.氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH﹣)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写不正确的是
A. 氯化铁与铁粉:Fe 3+ +Fe === 2Fe2+
B. 金属钠与水:2Na + 2H2O === 2Na+ + 2OH- + H2↑
C. 稀盐酸与碳酸钙:CaCO3 + 2H+ === Ca2+ + CO2 ↑ + H2O
D. 铜与浓硝酸:Cu + 4H++ 2NO3- ![]() Cu2++2NO2↑ +2H2O
Cu2++2NO2↑ +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池的说法不正确的是( )
A.手机上用的锂离子电池属于二次电池
B.铁件上镀铜,镀件连接电源的正极,用含Cu2+的盐溶液作电解质溶液
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图.图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( ) 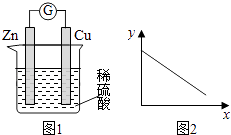
A.铜棒的质量
B.c(Zn2+)
C.c(H+)
D.c(SO42﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要从乙酸的乙醇溶液中回收乙酸,合理的操作组合是( ) ①蒸馏 ②过滤 ③静置分液 ④加足量钠 ⑤加入足量H2SO4 ⑥加入足量NaOH溶液 ⑦加入乙酸与浓H2SO4混合液后加热 ⑧加入浓溴水.
A.⑦③
B.⑧⑤②
C.⑥①⑤②
D.⑥①⑤①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com