
【题目】羰基硫(COS)在常温常压下为有臭鸡蛋气味的无色气体,广泛应用于农药、医药和其他化工生产中,存在于煤、石油和天然气中的羰基硫会腐蚀设备、污染环境,更会危害人体健康,工业上处理羰基硫常见的方法有水解反应和氢解反应。
(1)已知羰基硫中所有原子最外层均达到8电子结构,则其结构式为________________。
(2)①已知:H2(g)+COS(g)![]() H2S(g)+CO(g)△H1=+6.2kJ·mol-1;
H2S(g)+CO(g)△H1=+6.2kJ·mol-1;
②H2(g)+CO2(g)![]() H2O(g)+CO(g)△H2=+41.2kJ·mol-1;
H2O(g)+CO(g)△H2=+41.2kJ·mol-1;
则COS水解反应的热化学方程式为H2O(g)+COS(g)=H2S(g)+CO2(g),△H=___________kJ/mol.
②已知:COS水解反应的机理如下,其中吸附在催化剂表面的物种用*标注。
a. 吸附:H2O→H2O*
b. 反应:COS+H2O*→CO2+H2S*
c. 脱附:H2S*→H2S
已知COS水解反应的反应速率由b决定,则a、b、c三步中活化能最大的是__________________。
(3)已知COS氢解反应的热化学方程式为H2(g)+COS(g)![]() H2S(g)+CO(g) △H=+6.2kJ·mol-1,一定温度下,向某恒容密闭容器中充入4molCOS(g)和6molH2(g)发生氢解反应,H2、COS的体积分数
H2S(g)+CO(g) △H=+6.2kJ·mol-1,一定温度下,向某恒容密闭容器中充入4molCOS(g)和6molH2(g)发生氢解反应,H2、COS的体积分数![]() 随时间变化的关系如图所示,
随时间变化的关系如图所示,
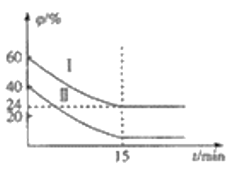
①H2的平衡转化率为_________________,
②该温度下,反应的平衡常数K为__________________,
③其他条件不变,20min时,向该容器中充入2molH2和3molCO,此时v(正)______________v(逆)(填“大于”“小于”或“等于”)。
【答案】O=C=S -35.0 b 60% 13.5 等于
【解析】
(2)根据盖斯定律进行计算;
②化学反应的反应速率由反应速率最慢的一步决定,且反应的活化能越大,反应速率越慢;
(3)根据已知信息和反应的特点,列三段式进行计算。
(1)已知羰基硫中所有原子最外层均达到8电子结构,类比CO2,可知其结构式为O=C=S;
(2)已知热化学方程式:①H2(g)+COS(g)![]() H2S(g)+CO(g)△H1=+6.2kJ·mol-1;②H2(g)+CO2(g)
H2S(g)+CO(g)△H1=+6.2kJ·mol-1;②H2(g)+CO2(g)![]() H2O(g)+CO(g)△H2=+41.2kJ·mol-1;根据盖斯定律可知,由①-②可得目标方程式,则COS水解反应的热化学方程式为H2O(g)+COS(g)=H2S(g)+CO2(g) △H=△H1-△H2=+6.2kJ·mol-1 - 41.2kJ·mol-1= -35.0kJ/mol;
H2O(g)+CO(g)△H2=+41.2kJ·mol-1;根据盖斯定律可知,由①-②可得目标方程式,则COS水解反应的热化学方程式为H2O(g)+COS(g)=H2S(g)+CO2(g) △H=△H1-△H2=+6.2kJ·mol-1 - 41.2kJ·mol-1= -35.0kJ/mol;
②已知COS水解反应的反应速率由b决定,则步骤b的反应速率最慢,则a、b、c三步中活化能最大的是b;
(3)该反应前后气体物质的量不变,则气体总物质的量始终为10mol,由图像可知,达到平衡状态时,H2(g)的体积分数为24%,则平衡时,H2(g)的物质的量为2.4mol,则H2(g)的转化量为3.6mol,
①则H2的平衡转化率为![]() ;
;
②可列出三段式为(单位为mol):
 ,因为该反应前后气体物质的量不变,故该温度下,反应的平衡常数
,因为该反应前后气体物质的量不变,故该温度下,反应的平衡常数![]() ;
;
③其他条件不变,20min时,向该容器中充入2molH2和3molCO,此时n(H2)=4.4mol,n(CO)=6.6mol,则浓度商![]() ,故反应处于平衡状态,则v(正)等于v(逆)。
,故反应处于平衡状态,则v(正)等于v(逆)。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 为短周期主族元素,其常见化合价与原子半径的关系如图所示。已知四种元素中只有 Y 与 Z 同周期,下列说法正确的是( )
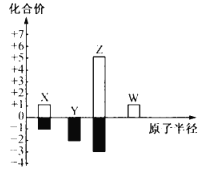
A.简单氢化物的稳定性:Y<Z
B.X、Y、Z 可组成盐类化合物
C.X 的氧化物中不可能含非极性键
D.W 的最高价氧化物对应水化物为弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用CO、H2制造CH3OCH3有三个途径:
CO(g)+H2(g)═CH3OH(g) △H1=-91kJmol-1 平衡常数K1
2CH3OH(g)═CH3OCH3(g)+H2O △H2=-24kJmol-1 平衡常数K2
CO(g)+H2O(g)═CO2(g)+H2(g) △H3=-41kJmol-1 平衡常数K3
新工艺的总反应式为3CO(g)+3H2(g)═CH3OCH3(g)+CO2(g)则该反应的△H=_____,化学平衡常数为K=__(用K1、K2、K3的代数式表示);
(2)一定条件下气体A与气体B反应生成气体C,反应过程中反应物与生成物的浓度随时间变化的曲线如图.此反应在达到平衡时,A的转化率为__;

(3)研究减少有毒气体的排放对改善环境消除雾霾有十分重要的意义。利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)5CO2(g)+I2(s) △H。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如图。

请回答:
①该反应属于__反应(填“放热”或“吸热“);
②从反应开始至a点时的反应速率为v(CO)=___,b点时化学平衡常数Kb=__;
③下列说法不正确的是____(填字母序号)。
a.容器内气体密度不变,表明反应达到平衡状态
b.两种温度下,c点时体系中混合气体的压强相等
c.增大d点的体系压强,CO的转化率不变
d.b点和d点的化学平衡常数:Kb<Kd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6可用作高压电力设备中的“气体绝缘开关”,由S(g)与F2(g)制备SF6(g)的能量变化如图所示,下列说法正确的是
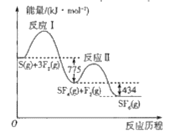
A.若已知S-F键的键能则可确定F-F键的键能
B.S(g)+3F2(g)=SF6(g)△H=+1209kJ·mol-1
C.与S(g)+3F2(g)=SF6(g)相比,S(s)+3F2(g)=SF6(g)放出的热量较多
D.由于反应Ⅰ放出的热量大于反应Ⅱ,所以反应速率:Ⅰ>Ⅱ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计如下两个实验证明:①氧化性:Fe3+>I2,②反应2Fe3++2I-=2Fe2++I2为可逆反应,下列说法中错误的是
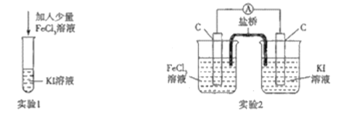
A.实验1试管中加入淀粉后溶液变蓝,该条件下氧化性:Fe3+>I2
B.实验2中最后电流表指针不再偏转可证明上述反应为可逆反应
C.实验1反应结束后,向试管中加入KSCN能判断该反应是否为可逆反应
D.实验2电流表指针不再偏转时,向右侧烧杯中加入单质碘可判断该反应是否为可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脑白金的主要成分的结构简式如图:
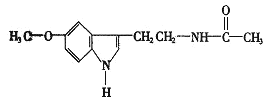
下列对脑白金主要成分的推论错误的是( )
A.其分子式为C13H16N2O2
B.能水解生成乙酸
C.能与溴水发生加成反应
D.其营养成分及官能团与葡萄糖相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.用FeCl3溶液腐蚀印刷电路板上铜箔:2Fe3++Cu=2Fe2++Cu2+
B.Fe与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
C.氢氧化钡溶液与硫酸反应:Ba2++![]() +OH-+H+=H2O+BaSO4↓
+OH-+H+=H2O+BaSO4↓
D.向小苏打溶液中滴入醋酸:![]() +2CH3COOH=CO2↑+H2O+2CH3COO-
+2CH3COOH=CO2↑+H2O+2CH3COO-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com