
【题目】下列各项中的两个量,其比值一定为1:2的是( )
A.液面在“0”刻度时,25mL碱式滴定管和50mL碱式滴定管所盛溶液的体积
B.在过氧化钠固体中,阴离子与阳离子的个数
C.将质量分数为a%的H2SO4溶液蒸发水后变为2a%,蒸发前后H2SO4溶液的物质的量浓度
D.在碳与浓硫酸(加热)的反应中,被还原的H2SO4与参加反应的H2SO4的物质的量
【答案】B
【解析】解:A.滴定管最大值下面还有溶液,且这部分溶液的体积未知,导致无法计算其溶液体积的比值,故A错误; B.过氧化钠中阴离子是过氧根离子,在过氧化钠固体中,阴离子与阳离子的个数之比为:1:2,故B正确;
C.依据C= ![]() 可知,若稀释过程中密度ρ保持不变,则质量分数为a%的H2SO4溶液蒸发水后变为2a%,蒸发前后H2SO4溶液的物质的量浓度之比为1:2,
可知,若稀释过程中密度ρ保持不变,则质量分数为a%的H2SO4溶液蒸发水后变为2a%,蒸发前后H2SO4溶液的物质的量浓度之比为1:2,
但是稀释过程中ρ变小,所以≠1:2,故C错误;
D.依据方程式C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O可知硫酸中硫元素化合价都降低,所以浓硫酸都做氧化剂,被还原的H2SO4与参加反应的H2SO4的物质的量相等,故D错误;
CO2↑+2SO2↑+2H2O可知硫酸中硫元素化合价都降低,所以浓硫酸都做氧化剂,被还原的H2SO4与参加反应的H2SO4的物质的量相等,故D错误;
故选:B.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,分析其元素的填充规律,判断下列说法正确的是( ) 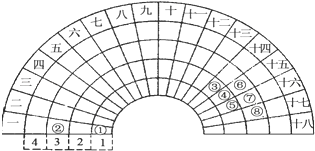
A.③元素形成的单质晶体均属于原子晶体
B.④元素的气态氢化物易液化,是因为其分子间存在氢键
C.②、⑦、⑧对应的简单离子半径依次减小
D.②⑤⑦三种元素形成的盐溶液在25℃时的pH值为7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知糖元(C6H10O5)n是一种相对分子质量比淀粉更大的多糖,主要存在肝脏和肌肉中,所以又叫动物淀粉和肝糖。下列关于糖元说法正确的( )
A.糖元、淀粉、纤维素互为同分异构体
B.糖元与淀粉、纤维素属于同系物
C.糖元水解的最终产物是葡萄糖
D.糖元具有还原性,能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上冶炼金属一般用热分解法、热还原法和电解法。你认为选择方法的主要依据是( )。
A. 金属在自然界的存在形式B. 金属元素在地壳中的含量
C. 金属熔点高低D. 金属阳离子得电子的能力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一个可逆反应,若正反应为自发过程,则其逆反应为非自发过程,反之亦然。
(1)已知2CO(g)![]() CO2(g)+C(s),T=980 K时ΔH-TΔS=0。当体系温度低于980 K时,估计ΔH-TΔS________0(填“大于”、“小于”或“等于”,下同);当体系温度高于980 K时,估计ΔH-TΔS________0。
CO2(g)+C(s),T=980 K时ΔH-TΔS=0。当体系温度低于980 K时,估计ΔH-TΔS________0(填“大于”、“小于”或“等于”,下同);当体系温度高于980 K时,估计ΔH-TΔS________0。
(2)电子工业中清洗硅片上的SiO2(s)的反应为SiO2(s)+4HF(g)===SiF4(g)+2H2O(g) ΔH(298.15 K)=-94.0 kJ/mol,ΔS(298.15 K)=-75.8 J/(mol·K),设ΔH和ΔS不随温度而变化,则此反应自发进行的温度是________。
(3)化学反应2NO(g)+2CO(g)===N2(g)+2CO2(g)在298 K、100 kPa下:ΔH=-113.0 kJ/mol,ΔS=-145.3 J/(mol·K),反应在常温下________(填“能”或“不能”)自发进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生使用托盘天平称食盐时,错误的将食盐放在右托盘,而把砝码放在左托盘,称得食盐的质量为15.5g(1g以下只能使用游码)。.如果按正确的方法,食盐的质量应为
A. 15.5g B. 15.0g C. 14.5g D. 14.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象正确的是( )
A.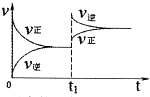
反应的正方向放热(t1时升温)
B.
SO2气体通入氯水中
C.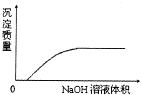
NaOH溶液滴加Ca(HCO3)2溶液中
D.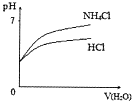
将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com