
分析 Al和NaOH溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据转移电子守恒计算生成氢气的物质的量,再根据V=nVm计算生成氢气体积.
解答 解:n(Al)=$\frac{5.4g}{27g/mol}$=0.2mol,Al和NaOH溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据转移电子守恒得生成氢气物质的量=$\frac{0.2mol×3}{2}$=0.3mol,生成氢气体积=0.3mol×22.4L/mol=6.72L,
故答案为:0.3mol;6.72L.
点评 本题考查物质的量的有关计算,为高频考点,明确各个物理量的关系是解本题关键,注意转移电子守恒的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
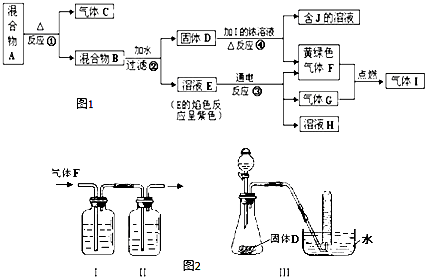
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②④⑤ | C. | ①③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、SO42-、OH- | B. | Ca2+、Na+、NO3-、CO32- | ||
| C. | Na+、H+、CO32-、Cl- | D. | Na+、Cl-、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
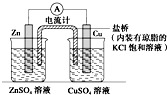
| A. | 该装置中电子由Zn极流向Cu极,CuSO4溶液中的SO41-通过盐桥移向Zn极 | |
| B. | 若装置中的两烧杯中均为CuSO4溶液,则电流计的指针偏转幅度变小,且很快减弱 | |
| C. | 将装置中烧杯内的溶液对换,电流计的指针也能发生偏转 | |
| D. | 将盐桥改为铜导线连接两种溶液,电流方向为由Cu极到Zn极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
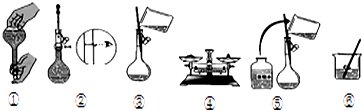
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com