
【题目】从有机物A开始有如图所示的转化关系(部分产物略去).A在NaOH溶液中水解生成B、C和D,1molF与足量的新制Cu(OH)2碱性悬浊液加热充分反应可生成2mol红色沉淀.分析并回答问题: 
(1)A中含有的官能团为氯原子(﹣Cl)和、;
(2)指出反应类型:A→B、C、D; H→I;
(3)写出下列反应的化学方程式:
①C→F:;②E→H:;
(4)与E含有相同官能团的某有机物甲(C4H8O3)有多种同分异构体,在结构中含有酯基和羟基,且水解产物不存在两个羟基连在同一个碳上的同分异构体有种.
【答案】
(1)酯基;羟基
(2)水解反应或取代反应;加聚反应
(3)![]() +O2
+O2 ![]() ?
? ![]() +2H2O;
+2H2O;![]()
(4)7
【解析】解:A在NaOH溶液中水解生成B、C和D,发生了酯的水解和卤代烃的水解,B酸化得到E,故E中含有羧基,E转化为H,H在一定条件下反应生成I,反应前后各元素的组成比不变,说明H转化I应为加聚反应,则H中含有C=C,则H为CH2=CHCOOH,I为 ![]() ,E发生酯化反应成八元环状化合物生成M,可知E为HOCH2CH2COOH,M为
,E发生酯化反应成八元环状化合物生成M,可知E为HOCH2CH2COOH,M为  ,B为HOCH2CH2COONa,A在碱性条件下生成HOCH2CH2COONa、NaCl和C,D与硝酸银、硝酸反应得到白色沉淀G,故D为NaCl,G为AgCl.C的分子式为C4H10O2 , 分子中含有甲基,由C催化氧化生成F(C4H6O2),1molF(C4H6O2)与足量新制的Cu(OH)2在加热条件下充分反应可生成2molCu2O,则F分子中含有2个﹣CHO,故C为
,B为HOCH2CH2COONa,A在碱性条件下生成HOCH2CH2COONa、NaCl和C,D与硝酸银、硝酸反应得到白色沉淀G,故D为NaCl,G为AgCl.C的分子式为C4H10O2 , 分子中含有甲基,由C催化氧化生成F(C4H6O2),1molF(C4H6O2)与足量新制的Cu(OH)2在加热条件下充分反应可生成2molCu2O,则F分子中含有2个﹣CHO,故C为 ![]() ,F为
,F为 ![]() ,所以有机物A为
,所以有机物A为 ![]() 或
或 ![]() .
.
(1.)由上述分析可知,A为 ![]() 或
或 ![]() ,含有官能团为:酯基﹣COOC﹣、羟基﹣OH、氯原子﹣Cl,所以答案是:酯基;羟基;
,含有官能团为:酯基﹣COOC﹣、羟基﹣OH、氯原子﹣Cl,所以答案是:酯基;羟基;
(2.)A在碱性条件下发生水解反应生成B、C、D,也属于取代反应;H→I是CH2=CHCOOH发生加聚反应生成 ![]() ,所以答案是:水解反应或取代反应;加聚反应;
,所以答案是:水解反应或取代反应;加聚反应;
(3.)①C→F的反应方程式为: ![]() +O2
+O2 ![]()
![]() +2H2O,②E→H的反应方程式为:
+2H2O,②E→H的反应方程式为: ![]() ,
,
所以答案是: ![]() +O2
+O2 ![]()
![]() +2H2O;
+2H2O; ![]() .
.
(4.)E为HOCH2CH2COOH,与E含有相同官能团的某有机物甲(C4H8O3)有多种同分异构体,在结构中含有酯基和羟基,且水解产物不存在两个羟基连在同一个碳上的同分异构体有HOCH2CH2COOCH3、CH3CH(0H)COOCH3、CH


科目:高中化学 来源: 题型:
【题目】合理膳食、合理用药是人体健康的需要. ①下列营养素中,不能对人体提供能量的是(填字母).
a.维生素 b.糖类 c.蛋白质
②某肉制品包装上印有相关配料如图所示.
其中属于调味剂的是;属于发色剂的是;
属于防腐剂的是 .
③当体内胃酸分泌过多时,医生会建议服用以下常用药物中的(填字母).
a.阿司匹林 b.青霉素片 c.复方氢氧化铝片 d.合成抗菌药.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸二乙酯是乙酸纤维素、硝酸纤维素的增塑剂,实验室合成己二酸二乙酯的反应原理和有关数据如下: ![]() +2C2H5OH
+2C2H5OH ![]()
![]() +2H2O
+2H2O
相对分子质量 | 密度/(gcm﹣3) | 沸点/℃ | 水中溶解性 | |
己二酸二乙酯 | 202 | 1.01 | 245 | 不溶于水 |
己二酸 | 146 | 1.36 | 231.8 | 微溶 |
乙醇 | 46 | 0.79 | 78.4 | 混溶 |
甲苯 | 92 | 0.87 | 110.6 | 不溶于水 |
实验步骤如下:
步骤1:在50mL圆底烧瓶中加入己二酸1.8g(0.012mol),乙醇4.4mL(0.076mol),甲苯5mL和浓硫酸(1mL),装置如图所示,小火加热回流40min.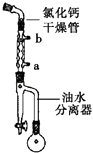
步骤2:冷却,回流装置改为蒸馏装置,常压蒸馏,在120℃左右充分蒸馏.
步骤3:将步骤2的液体倒入克氏烧瓶,进行减压蒸馏,最后得己二酸二乙酯2.2g.
(1)图中冷凝管中冷却水从(填“a”或“b”)口进,浓硫酸的主要作用是作催化剂 .
(2)回流一段时间后,打开图中旋塞,流出的物质主要是 .
(3)实验中加入过量的乙醇的目的是 .
(4)步骤2实验已完成的标志是 .
(5)本实验的产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为128的有机物A完全燃烧只生成CO2和H2O,若A含一个六碳环且可与NaHCO3溶液反应,则环上一氯代物的数目为( )
A.2
B.3
C.4
D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是

A. a点对应的溶液中:Na+、OH-、SO42-、NO3-
B. b点对应的溶液中:H+、Fe3+、MnO4-、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D. d点对应的溶液中:S2-、NO3-、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、D、E、G四种微粒组成的复盐W的化学式为xAaDdyE2DzG.4.704g W溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g.同质量的W与5.13g氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 0.624g,加热后的残渣用水充分溶解后过滤,滤液以酚酞为指示剂用0.400mol/L H2SO4滴定至终点,用去H2SO4 15.0mL,滴定完毕后,溶液中检测不出任何金属离子和酸根离子;滤渣用硝酸洗涤时部分溶解,得一遇石炭酸显紫色的黄色溶液,依据推理和计算判断:
(1)依次写出D、E、G三种微粒符号、、;
(2)a、d的比值为;
(3)复盐的化学式为 . (写出计算步骤)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的化工产品,工业上可以按照下图所示流程生产氨气: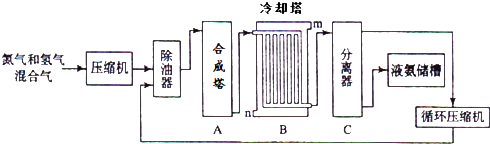
(1)原料气之一氮气的工业制取方法是 , 写出氨气的工业用途(任答一点) .
(2)写出合成塔中发生的反应的化学反应方程式 .
在冷却塔中对混合气体进行冷却,冷水的入口(答m或n).
(3)设备C的作用 .
其分离器中的过程对整个工业合成氨的意义 . (试结合平衡移动原理回答)
(4)在原料气制备过程中混有 CO对催化剂有毒害作用,欲除去原料气中的 CO,可通过如下反应来实现:CO(g)+H2O(g)CO2(g)+H2(g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过80%,则起始物中c(H2O):c(CO)不低于(精确到小数点后一位).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列相关离子方程式书写正确的是( )
A.NaClO溶液与FeCl2溶液混合:6Fe2++3ClO﹣+3H2O═2Fe(OH)3↓+3Cl﹣+4Fe3+
B.用食醋检验牙膏中的碳酸钙:CaCO3+2H+═Ca2++CO2↑+H2O
C.FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2═2Fe3++2H2O
D.电解MgCl2水溶液的离子方程式:2Cl﹣+2H2O ![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中错误的是
A. 气体摩尔体积约为22.4L/mol
B. 2 mol N2O和2 mol NO2含原子数相同
C. 等质量的O2和O3中所含氧原子个数相同
D. 等物质的量的CO和CO2中所含碳原子数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com