
����Ŀ��2012��11��ij����ҵ�����İƱ����ܻ�������267%���Ʋ�Ʒ�е��ܻ�����ҪԴ�����ϽӾ�Ͱ��������ƹܡ���Ʒ�������ڸǵȡ��ܻ���DEHP�ĺϳ���·���£�
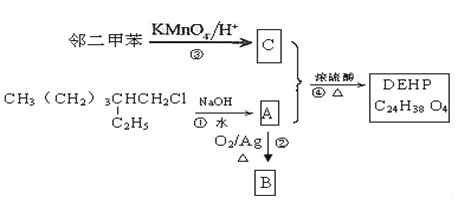
��1��A��ϵͳ����������Ϊ______________��C���Ӻ˴Ź���������ʾ��__________�ֲ�ͬ��ѧ��������ԭ�ӡ�C��һ�����������Ҷ�����Ӧ���ɵĸ߾�����һ����Ҫ�ĺϳ���ά���׳Ƶ��ڣ���ṹ��ʽ��__________��
��2��B���еĹ���������Ϊ__________���������ķ�Ӧ���ͷֱ�Ϊ_______��_______��
��3��д����������������C��ͬ���칹��Ľṹ��ʽ:____________��
a���DZ�����λ��Ԫȡ���b����FeCl3��Һ��ʾ������ɫ��
c������̼��������Һ��Ӧ
��4��д�����з�Ӧ�Ļ�ѧ����ʽ��
��Ӧ����_______________________________________________��
��Ӧ����_______________________________________________��
���𰸡�2-�һ�-1-�Ѵ� 3 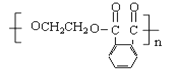 ȩ�� ȡ����Ӧ ������Ӧ
ȩ�� ȡ����Ӧ ������Ӧ 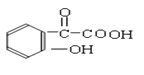
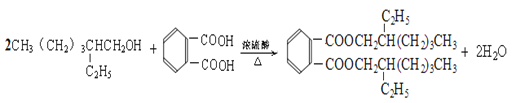
��������
�ڶ��ױ�����Ϊ�ڶ������ᣬ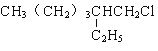 �ڼ���������ˮ�⣬��ԭ�ӱ��ǻ�ȡ�����õ�2-�һ�-1-�Ѵ������ڶ������ᷢ��������Ӧ�õ�
�ڼ���������ˮ�⣬��ԭ�ӱ��ǻ�ȡ�����õ�2-�һ�-1-�Ѵ������ڶ������ᷢ��������Ӧ�õ�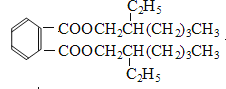 ��2-�һ�-1-�Ѵ�����������Ӧ�õ�
��2-�һ�-1-�Ѵ�����������Ӧ�õ�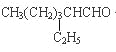 ��
��
��1��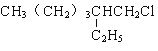 �ڼ���������ˮ�⣬��ԭ�ӱ��ǻ�ȡ�����õ�2-�һ�-1-�Ѵ���CΪ�ڶ������ᣬ��������3�ֲ�ͬ��ѧ��������ԭ�ӣ�C��һ�����������Ҷ�����Ӧ���ɵĸ߾�����һ����Ҫ�ĺϳ���ά���׳Ƶ��ڣ���ṹ��ʽ��
�ڼ���������ˮ�⣬��ԭ�ӱ��ǻ�ȡ�����õ�2-�һ�-1-�Ѵ���CΪ�ڶ������ᣬ��������3�ֲ�ͬ��ѧ��������ԭ�ӣ�C��һ�����������Ҷ�����Ӧ���ɵĸ߾�����һ����Ҫ�ĺϳ���ά���׳Ƶ��ڣ���ṹ��ʽ�� ��
��
��2��2-�һ�-1-�Ѵ�����������Ӧ�õ�BΪ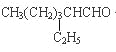 �����еĹ�����Ϊȩ������Ӧ��Ϊ±��������ȡ����Ӧ���ɴ�����Ӧ��Ϊ����������������ȩ��
�����еĹ�����Ϊȩ������Ӧ��Ϊ±��������ȡ����Ӧ���ɴ�����Ӧ��Ϊ����������������ȩ��
��3���ڶ��������ͬ���칹����������������a���DZ�����λ��Ԫȡ���b����FeCl3��Һ��ʾ������ɫ��˵�����з��ǻ���c������̼��������Һ��Ӧ��˵�������Ȼ�����ȷ���ṹʽΪ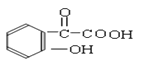 ��
��
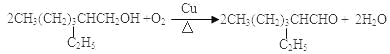
��4����Ӧ��Ϊ2-�һ�-1-�Ѵ�����������Ӧ�õ�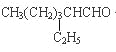 ����ѧ����ʽΪ
����ѧ����ʽΪ ����Ӧ��Ϊ2-�һ�-1-�Ѵ����ڶ������ᷢ��������Ӧ����DEHP����ѧ����ʽΪ
����Ӧ��Ϊ2-�һ�-1-�Ѵ����ڶ������ᷢ��������Ӧ����DEHP����ѧ����ʽΪ ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������зḻ��ʳƷ���������Դ��ҩ���ˮ����Դ�ȣ���ͼ��ʾ����
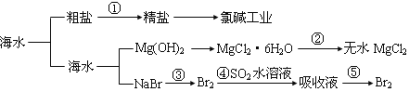
�����й�˵����ȷ���� (����)
A.�������г�ȥ�����е�SO42-��Ca2+��Mg2+��Fe3+�����ʣ������ҩƷ˳��Ϊ��Na2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������
B.��ҵ�Ͻ�������ͨ���ȼҵ��ȡ
C.�ڵ��ۢܢ�������Ԫ�ؾ�������
D.�ӵ���������������Ŀ����Ϊ��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���պ��㴼��������ʳ���㾫����ṹ��ʽ��ͼ1��ʾ��
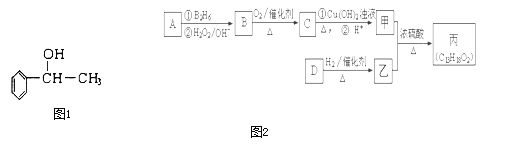
��֪��R-CH=CH2 ![]() R-CH2CH2OH
R-CH2CH2OH
![]() һ
һ![]() �պ��㴼�ķ���ʽΪ ______ �������ܷ������л���Ӧ������
�պ��㴼�ķ���ʽΪ ______ �������ܷ������л���Ӧ������![]() ���������
���������![]() ______ ��
______ ��
![]() ȡ����Ӧ
ȡ����Ӧ![]() �ӳɷ�Ӧ
�ӳɷ�Ӧ![]() ��ȥ��Ӧ
��ȥ��Ӧ![]() �Ӿ۷�Ӧ
�Ӿ۷�Ӧ![]() ������Ӧ
������Ӧ![]() ˮ�ⷴӦ��
ˮ�ⷴӦ��
![]() ��
��![]() �л������һ�����ϣ���ϳ�·����ͼ
�л������һ�����ϣ���ϳ�·����ͼ![]() ���м���Է�������ͨ���������Ϊ88�����ĺ˴Ź���������ʾֻ������壻�����պ��㴼��Ϊͬϵ�
���м���Է�������ͨ���������Ϊ88�����ĺ˴Ź���������ʾֻ������壻�����պ��㴼��Ϊͬϵ�
![]() ����ϵͳ��������A�������� ______ ��
����ϵͳ��������A�������� ______ ��
![]() ������
������![]() ����Һ��Ӧ�Ļ�ѧ����ʽΪ ______ ��
����Һ��Ӧ�Ļ�ѧ����ʽΪ ______ ��
![]() ���������
���к�������![]() ��D�ɷ���������Ӧ���ڴ���������1molD��2mol
��D�ɷ���������Ӧ���ڴ���������1molD��2mol![]() ���Է�Ӧ�����ң���D�Ľṹ��ʽΪ ______ ��
���Է�Ӧ�����ң���D�Ľṹ��ʽΪ ______ ��
![]() �����ҷ�Ӧ�Ļ�ѧ����ʽΪ ______ ��
�����ҷ�Ӧ�Ļ�ѧ����ʽΪ ______ ��
![]() ��������3��ȡ����������ţ����������Ե��ҵ�ͬ���칹�干�� _____ �֣�����3��ȡ����������Ż������ڵ��л���ṹ��ʽΪ ______ ��
��������3��ȡ����������ţ����������Ե��ҵ�ͬ���칹�干�� _____ �֣�����3��ȡ����������Ż������ڵ��л���ṹ��ʽΪ ______ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǽ���þ��±�ص���(X2)��Ӧ�������仯ʾ��ͼ�����������У���ȷ��˵���м��� �� ��

��Mg��s���������������MgX2��s�����������
��MgCl2�����Mg��s����Cl2��g�������ȹ���
�����ȶ��ԣ�MgI2��MgBr2��MgCl2��MgF2
�ܳ����������ԣ�F2��Cl2��Br2��I2
A. 1�� B. 2��
C. 3�� D. 4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݷ�Ӧ��2Ag+ + Cu = Cu2+ + 2Ag�������ͼ��ʾԭ��أ�����˵���������( )��
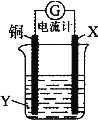
A.X����������ʯī
B.Y������ͭ��Һ
C.���Ӵ�ͭ�缫�����·����X�缫
D.X���ϵĵ缫��ӦʽΪAg+ + e��= Ag
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£����ܱ������г�������ʵ�����NO��CO��������Ӧ��2NO(g)+2CO(g)![]() N2(g)+2CO2(g)����������ѧ��Ӧ�ﵽƽ��ʱ������������ȷ���ǣ� ��
N2(g)+2CO2(g)����������ѧ��Ӧ�ﵽƽ��ʱ������������ȷ���ǣ� ��
A.CO2��CO�����ʵ���һ�����
B.NO��CO2�����ʵ���һ�����
C.��Ӧ���ת���ʴﵽ�˸������µ������
D.ƽ��ʱ�����������ʵ���һ�����ڷ�Ӧ��ʼǰ�����������ʵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������Ҫ�Ļ�������ԭ�ϣ��ɹ�ҵ��������(����Ba2+��Ca2+��Mg2+������)�Ʊ�������̼���ȵĹ����������£�
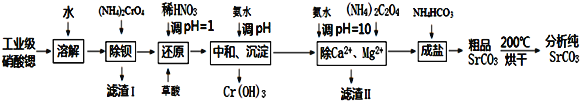
��֪����BaCrO4������ˮ����ˮ��Һ��Cr2O72-��Ba2+���ܽ�ϡ�
�ڳ����£������ʵ��ܻ��������±���ʾ��
������ | Ca(OH)2 | CaC2O4 | Mg(OH)2 | MgC2O4 | Cr(OH)3 |
Ksp����ֵ | 5.0��10-6 | 2.2��10-9 | 5.6��10-12 | 4.8��10-6 | 10-30 |
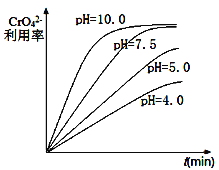
(1)��������������CrO42-�ڲ�ͬpHʱ����������ʱ��仯��������ͼ��ʾ������ͼ���������������������Ҫ����pH=7.5��ԭ��_______________________________��
(2)����ԭ�������У�Ӧ�ȵ���pH=1.0���ټ�����ᣬ�������ʱ������Ӧ�����ӷ���ʽΪ_____________________________��
(3)��������������Ҫ�ɷ�Ϊ________________��
(4)����Ca2+��Mg2+����õ�����Һ�г�����Sr(NO3)2����й�����NH3��H2O�����������������з�����Ӧ�����ӷ���ʽΪ__________________________��
(5)����ƷSrCO3����ɹ����г�ȥ����Ҫ����Ϊ_____________________��
(6)�����к͡������������У��ٶ���ʼCr3����Zn3+Ũ��Ϊ0.1mol/L��������pHΪ_______ʱ������ʼ�����������Ӽ������pHΪ_____ʱ�����պ���ȫ����(����Ũ��С��1��10-6mol/Lʱ��������Ϊ�����ӳ�����ȫ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����һ��Ũ�ȵ�Na2X��Һ�е������ᣬ��Һ��pH������Ũ�ȱ仯��ϵ��ͼ��ʾ��

��֪��H2X�Ƕ�Ԫ���ᣬY��ʾ![]() ��
��![]() ��pY����lgY��������������ȷ���ǣ�������
��pY����lgY��������������ȷ���ǣ�������
A. ����n��ʾpH��p![]() �ı仯��ϵ
�ı仯��ϵ
B. Ka2��H2X����1.0��10��10.3
C. NaHX��Һ��c��H+����c��OH����
D. ����Һ������ʱ��c��Na+����c��HX����+2c��X2����+c��Cl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��B��F�Ǽ�ͥ�г������л��F������ʳƷ��װ��E��ʯ�ͻ�����չˮƽ�ı�־����������ת����ϵ�ش����⡣

��1���ֱ�д��A��E�й����ŵ����ƣ�A��_________��E��_________��
��2��������������Ϊ________________��
��3��д����Ӧ���ͣ���_________��
��4����д�����з�Ӧ�Ļ�ѧ����ʽ��
��д��A��B��Ũ�����м��ȷ�Ӧ�ķ���ʽ_________________��
��B�ڽ���ͭ�������ڿ����м��ȷ�Ӧ________________��
��5��F��һ�ֳ����ĸ߷��Ӳ��ϣ��������Ǵ����˾�ķ��㡣Ȼ�������ֲ�����ɵĵ����ijһ����������__________________.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com