
| A. | 酯化反应也属于加成反应 | |
| B. | 酯化反应中羧酸脱去羧基中的氢原子,醇脱去羟基中的羟基生成水 | |
| C. | 浓硫酸在酯化反应中不只起催化剂的作用 | |
| D. | 欲使酯化反应生成的酯分离并提纯,可以将酯蒸气通过导管伸入饱和碳酸钠溶液的液面下,再用分液漏斗分离 |
分析 A.酯化反应中羧酸脱羟基、醇脱氢;
B.酯化反应中羧酸脱去羧基中OH;
C.浓硫酸具有吸水性,利用酯化反应正向进行;
D.乙醇、乙酸易溶于水,则导管伸入饱和碳酸钠溶液的液面下发生倒吸.
解答 解:A.酯化反应中羧酸脱羟基、醇脱氢,可看成醇中H被取代,为取代反应,故A错误;
B.酯化反应中羧酸脱去羧基中OH,醇脱去羟基中H,故B错误;
C.浓硫酸具有吸水性,利用酯化反应正向进行,则浓硫酸作催化剂、吸水剂,故C正确;
D.乙醇、乙酸易溶于水,则导管伸入饱和碳酸钠溶液的液面下发生倒吸,导管口应在液面上,分层后利用分液漏斗分离,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握酯化反应实验、有机物的性质、混合物分离提纯为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | SO2+H2O→H2SO3 | B. | Cl2+H2O→HCl+HClO | ||
| C. | 2F2+2H2O→4HF+O2 | D. | 2Na+2H2O→2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 密度/(g•mL-1) | 沸点 | 水溶性 | 溶解性 |
| 甲 | 0.893 | 78.5℃ | 溶 | 溶于乙 |
| 乙 | 1.220 | 100.7℃ | 溶 | 溶于甲 |
| A. | 萃取 | B. | 分液 | C. | 过滤 | D. | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
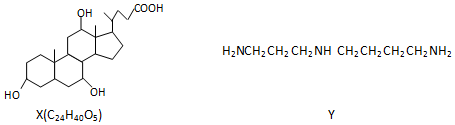
| A. | 1molX在浓硫酸作用下发生消去反应,最多生成3molH2O | |
| B. | 1molY发生类似酯化的反应,最多消耗2molX | |
| C. | X与足量HBr反应,所得有机物的分子式为C24H37O2Br3 | |
| D. | Y与癸烷的分子链均呈锯齿形,但Y的极性较强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2与NaOH溶液完全反应,转移电子数为2NA | |
| B. | 100g36.5%的盐酸中含HCl分子为NA | |
| C. | 1.12LCl2含有1.7NA个质子 | |
| D. | 56gFe与足量的Cl2完全反应,消耗Cl2分子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )| 选项 | W | X |
| A | 盐酸 | Na2CO3溶液 |
| B | NaOH溶液 | AlCl3溶液 |
| C | CO2 | Ca(OH)2溶液 |
| D | Cl2 | Fe |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com