


分析 MgCl2、AlCl3的混合溶液与过量氨水反应生成氢氧化镁和氢氧化铝沉淀,再经过过滤、洗涤、干燥得氢氧化镁和氢氧化铝沉淀,再在高温焙烧得到MgAl2O4固体,(1)先加入氨水,再加入盐的混合溶液,会使两种沉淀同时生成;
(2)根据题意可知,沉淀中应该附着氯离子和铵根离子,若判断是否洗净,可以取少量最后一次洗涤液,加入硝酸酸化的硝酸银溶液进行判断,若生成白色沉淀,则说明没有洗涤干净;若没有沉淀生成,则说明已经洗涤干净;
(4)根据所给的装置图可知,B中的饱和食盐水是为了除去混有的HCl气体;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收空气中的CO2,所以可以加入碱石灰来代替F和G的作用.
解答 解:(1)如先加入MgCl2、AlCl3的混合溶液,再加氨水,氨水少量,应先生成氢氧化镁沉淀,反之,先加氨水,因氨水足量,则同时生成沉淀,
故答案为:B;
(2)沉淀中应该附着氯离子和铵根离子,若判断是否洗净,可以取少量最后一次洗涤液,加入AgNO3溶液(或硝酸酸化的AgNO3溶液)溶液进行判断,若生成白色沉淀,则说明没有洗涤干净;若没有沉淀生成,则说明已经洗涤干净,
故答案为:AgNO3溶液(或硝酸酸化的AgNO3溶液);
(3)高温焙烧固体应在坩埚中进行,反应的化学方程式为:Mg(OH)2+2Al(OH)3=MgAl2O4+4H2O,
故答案为:坩埚; Mg(OH)2+2Al(OH)3=MgAl2O4+4H2O;
(4)B中的饱和食盐水是为了除去混有的HCl气体;因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,而G是吸收反应剩余的氯气,所以可以加入碱石灰来代替F和G的作用,
故答案为:除去HCl;吸收水蒸气;碱石灰.
点评 本题考查物质的制备实验设计,题目难度中等,注意把握实验设计的仪器连接顺序,清楚实验原理.


科目:高中化学 来源: 题型:选择题
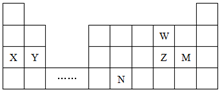
| A. | 原子半径:Y>Z>W | |
| B. | 单质的还原性:X>Y | |
| C. | 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料 | |
| D. | 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室中金属钠通常保存在煤油里 | |
| B. | 液溴易挥发,在存放液溴的试剂瓶中应加水封 | |
| C. | 保存FeCl3溶液时,通常在溶液中加少量的单质铁 | |
| D. | 浓硝酸通常保存在棕色试剂瓶中,置于阴凉处 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Fe溶于过量稀硝酸,电子转移数为2NA | |
| B. | 标准状况下,2.24L CCl4含有分子的数目为0.1NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1L 0.1mol/L的NaHCO3溶液中,HCO3-、CO32-离子数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属.目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属.目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
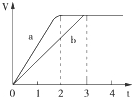 在一定温度和压强下,使Mg和Zn分别与等浓度、等体积的过量稀盐酸反应,产生气体的体积(V)与反应时间(t)的关系如图所示.下列叙述正确的是( )
在一定温度和压强下,使Mg和Zn分别与等浓度、等体积的过量稀盐酸反应,产生气体的体积(V)与反应时间(t)的关系如图所示.下列叙述正确的是( )| A. | 曲线a代表的是Zn的反应,曲线b代表的是Mg的反应 | |
| B. | 两个反应分别在2min、3min时达到化学平衡 | |
| C. | Mg和Zn的反应速率之比为3:2 | |
| D. | 用Fe代替Zn,其他条件不变,绘出的图象完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚、苯乙醇和苯乙酸都可以与钠反应生成氢气 | |
| B. | 受羟基的影响,苯环上的氢变得活泼,苯酚的溴代比苯的溴代更容易 | |
| C. | 用酸性高锰酸钾溶液可以鉴别苯和甲苯 | |
| D. | 纤维素、蔗糖、葡萄糖在一定条件下都可发生水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com