
| A、若在恒温恒压下,当x=1时,按1.5 mol A、1 mol C作为起始物质,达到平衡后,C的体积分数仍为a |
| B、若在恒温恒容下,当x=2时,将2molC作起始物质,达到平衡后,C的体积分数仍为a |
| C、若在恒温恒压下,当x=3时,1mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为a |
| D、若在恒温恒容下,按0.6mol A、0.3mol B、1.4mol C作起始物质,达到平衡后,C的体积分数仍为a,则x一定为2或3 |


科目:高中化学 来源: 题型:
| A、容器中已肯定无Fe粉存在 |
| B、容器中可能有Cu粉存在 |
| C、溶液中Fe2+比Cu2+多 |
| D、溶液中肯定不存在Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制取肥皂时,常常加入少量乙醇,目的是加快皂化反应 |
B、海水提镁的主要步骤为: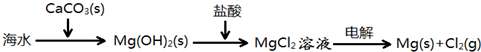 |
| C、工业上将二氧化碳和氨气通入食盐水中制的碳酸氢钠,再煅烧碳酸氢钠使其转化为碳酸钠 |
| D、用蒸馏法便可分离苯和溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6molA+2molB |
| B、1.5molA+0.5molB+1molC+0.5molD |
| C、3molA+1mol B+2molC+1molD |
| D、2molC+1molD |
查看答案和解析>>
科目:高中化学 来源: 题型:
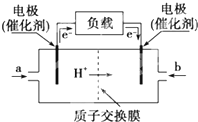 如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列有关该电池的说法错误的是( )
如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图.甲醇在催化剂作用下提供质子(H+)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列有关该电池的说法错误的是( )| A、右边的电极为电池的负极,b处通入的是空气 |
| B、左边的电极为电池的负极,a处通入的是甲醇 |
| C、电池负极的反应式为:2CH3OH+2H2O-12e-═2CO2↑+12H+ |
| D、电池正极的反应式为:3O2+12H++12e-═6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的铝分别与盐酸和氢氧化钠溶液反应生成氢气的物质的量 |
| B、1 mol/L KI与0.5 mol/L K2CO3溶液中的K+数目 |
| C、质量比为3:4的金刚石和石墨中的碳碳键数目 |
| D、常温下,pH均为3的HNO3与Fe(NO3)3溶液中,由水电离产生的c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com