
| A. | 热稳定性:HCl>HI | B. | O2和O3互为同素异形体 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 干冰和冰为同一种物质 |
分析 A.非金属性越强,对应氢化物越稳定;
B.O2和O3为同种元素的不同单质;
C.非金属性越强,对应最高价含氧酸的酸性越强;
D.干冰为固体二氧化碳,而冰为水.
解答 解:A.非金属性Cl>I,热稳定性:HCl>HI,故A正确;
B.O2和O3为同种元素的不同单质,二者互为同素异形体,故B正确;
C.非金属性Cl>S>P>Si,则酸性:HClO4>H2SO4>H3PO4>H2SiO3,故C正确;
D.干冰为固体二氧化碳,而冰为水,二者为不同物质,故D错误;
故选D.
点评 本题考查周期表和周期律的应用,为高频考点,把握元素的性质、元素周期律及物质组成和关系为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案科目:高中化学 来源: 题型:实验题
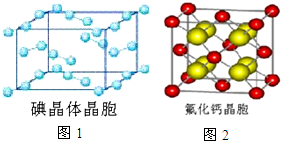 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | B. | 次氯酸的结构式:H-O-Cl | ||
| C. | NH4Cl的电子式: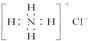 | D. | 硝基苯的结构简式: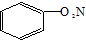 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取8.75 g食盐 | |
| B. | 用25 mL量筒量取12.36 mL盐酸 | |
| C. | 用广泛pH试纸测得某溶液pH值为3.5 | |
| D. | 用碱式滴定管移取NaOH溶液23.10 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | H2CO3 | HClO | HAlO2 |
| 电离常数 (25℃) | Ka1=4.4×10-7 | Ka=3×10-8 | Ka=6.3×10-13 |
| Ka2=4.7×10-11 |
| A. | NaClO溶液中通入过量CO2:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | NaAlO2溶液中加入过量CO2:AlO2-+CO2+2H2O═HCO3-+Al(OH)3↓ | |
| D. | NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═CO32-+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
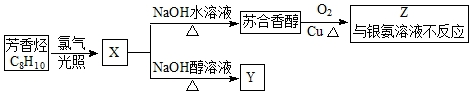
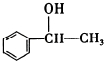 ,它不能发生的有机反应类型有④、⑥.
,它不能发生的有机反应类型有④、⑥.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
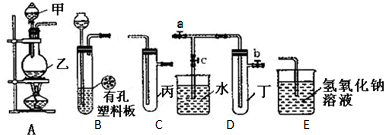
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L CCl4中含有共价键的数目为0.4 NA | |
| B. | 常温下,9.2 g NO2和N2O4的混合气体中含有氮原子的数目为0.2 NA | |
| C. | 电解精炼铜时,若阳极质量减少64g,则阴极得到电子的数目为2 NA | |
| D. | 0.1mol苯乙烯中含有碳碳双键的数目为0.4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com