
A、B、C、D、E这五个集气瓶,分别装有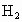 、
、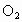 、
、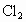 、HCl、HBr五种气体,其中A和D混合见强光即爆炸,B和A混合在瓶壁上出现红棕色小液滴,打开E的瓶盖,在潮湿的空气中会出现白雾.根据上述现象推断它们的化学式:
、HCl、HBr五种气体,其中A和D混合见强光即爆炸,B和A混合在瓶壁上出现红棕色小液滴,打开E的瓶盖,在潮湿的空气中会出现白雾.根据上述现象推断它们的化学式:
A__________,B__________,C_________,D_________,E__________.
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
| 3 | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+ Mg2+ Al3+ Ba2+ Fe3+ | ||||||
| 阴离子 | OH- Cl- CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
A、B、C、D、E这五个集气瓶,分别装有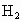 、
、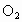 、
、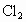 、HCl、HBr五种气体,其中A和D混合见强光即爆炸,B和A混合在瓶壁上出现红棕色小液滴,打开E的瓶盖,在潮湿的空气中会出现白雾.根据上述现象推断它们的化学式:
、HCl、HBr五种气体,其中A和D混合见强光即爆炸,B和A混合在瓶壁上出现红棕色小液滴,打开E的瓶盖,在潮湿的空气中会出现白雾.根据上述现象推断它们的化学式:
A__________,B__________,C_________,D_________,E__________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com