
ЁОЬтФПЁПШЫУЧУПЬьЖМвЊЩуШыДѓСПЕФЕэЗлРрЮяжЪЃЌвдЮЌГжЛњЬхЕФгЊбјОљКтЁЃетЪЧвђЮЊЕэЗл[ЛЏбЇЪНЮЊ(C6H10O5)n]дкЕэЗлУИзїгУЯТЛђдкЫсадЛЗОГЯТПЩвдЫЎНтГЩЦЯЬбЬЧ[ЛЏбЇЪНЪЧC6H12O6]ЃЌЧыМЦЫуЃК
(1)ЕэЗлЕФФІЖћжЪСПЮЊ______________ЃЛ
(2)НЋ90 gЦЯЬбЬЧШмгкЫЎЃЌХфГЩ1 LШмвКЃЌЫљЕУШмвКШмжЪЕФЮяжЪЕФСПХЈЖШЮЊ______________ЃЛ
(3)АбЕэЗлШмгкЗаЫЎжаЃЌжЦГЩЕэЗлШмвКЃЌЛиД№ЯТСаЮЪЬтЁЃ
ЂйШчКЮЭЈЙ§ЪЕбщжЄУїЕэЗлШмвКЪЧНКЬхЃК______________(ЬюЯжЯѓУћГЦ)ЁЃ
ЂкдкЕэЗлШмвКжаМгШыЩйСПТШЛЏФЦОЇЬхЃЌВЂзАШыАыЭИФЄДќЃЌЯЕНєДќПкЃЌАбЫќаќЙвдкЪЂгаеєяжЫЎЕФЩеБРяГфЗжЗДгІЁЃФмДгАыЭИФЄРяЮіГіЕФЗжЩЂжЪЕФЛЏбЇЪНЪЧ____________ЃЌИУВйзїЕФУћГЦЪЧ____________ЁЃ
(4)ЯТСаУшЪіЕФЗжБ№ЪЧНКЬхЕФаджЪЛђЯжЯѓЃЌЧыАДвЊЧѓЬюПеЃК
ЂйНКгШыКЃПкШ§НЧжоЕФаЮГЩЃЌетЪЧЗЂЩњСЫНКЬхЕФ_________ЃЛ
ЂкдкЭСШРЩЯЪЉгУКЌЕЊСПЯрЭЌЕФЬМЫсЧтяЇКЭЯѕЫсяЇЗЪСЯЃЌЬМЫсЧтяЇЗЪаЇИпЃЌетЪЧвђЮЊ_________________________________ЁЃ
ЂлгУКЌ0.1 mol FeCl3ЕФБЅКЭ FeCl3ШмвКжЦFe(OH)3НКЬхЪБЃЌаЮГЩНКЬхСЃзгЪ§ФПаЁгк0.1 NAЃЌетЪЧвђЮЊ_________________________________ЁЃ
ЁОД№АИЁП162ng/mol 0.5 mol/L ЖЁДяЖћаЇгІ NaCl ЩјЮі ОлГС ЭСШРНКЬхНКСЃДјИКЕчЃЌЖдNH4+ОпгаЮќИНзїгУЃЌПЩвдМѕЛКЦфСїЪЇ гЩгкНКСЃЪЧаэЖрИіFe(OH)3ЗжзгЕФОлМЏЬхЃЌЫљвдКЌга0.1 mol FeCl3ЕФБЅКЭШмвКжЦШЁFe(OH)3ЪБЃЌаЮГЩЕФНКСЃЪ§ФПаЁгк0.1 NA
ЁОНтЮіЁП
ЃЈ1ЃЉФІЖћжЪСПдкЪ§жЕЩЯЕШгкЯрЖдЗжзгжЪСПЃЛ
ЃЈ2ЃЉХЈЖШЮЊ![]() ЃЛ
ЃЛ
ЃЈ3ЃЉЂйПЩвдЭЈЙ§ЖЁДяЖћаЇгІМьВтЪЧЗёЪєгкНКЬхЃЌ
ЂкРћгУАыЭИФЄНјааЩјЮіПЩвдЬсДПНКЬхЃЌНКЬхЮЂСЃВЛФмЭИЙ§АыЭИФЄЃЌШмвКСЃзгПЩвдЭИЙ§АыЭИФЄЃЛ
ЃЈ4ЃЉЂйШ§НЧжоЕФаЮГЩЪЧгЩгкНКЬхОлГСдьГЩЕФЃЛ
ЂкЭСШРНКЬхНКСЃДјИКЕчЃЌЖд![]() ОпгаЮќИНзїгУЃЛ
ОпгаЮќИНзїгУЃЛ
Ђл![]() НКЬхжаЕФНКСЃЪЧаэЖрИі
НКЬхжаЕФНКСЃЪЧаэЖрИі![]() ЗжзгЕФОлМЏЬхЁЃ
ЗжзгЕФОлМЏЬхЁЃ
ЃЈ1ЃЉ![]() ЕФФІЖћжЪСПЮЊЃК162ng/molЃЛ
ЕФФІЖћжЪСПЮЊЃК162ng/molЃЛ
Д№АИЮЊЃК162ng/molЃЛ
ЃЈ2ЃЉ90 gЦЯЬбЬЧЕФЮяжЪЕФСПЮЊЃК![]() ЃЌХЈЖШЮЊ
ЃЌХЈЖШЮЊ![]() ЃЛ
ЃЛ
Д№АИЮЊЃК0.5 mol/LЃЛ
ЃЈ3ЃЉЂйПЩвдЭЈЙ§ЖЁДяЖћаЇгІМьВтЪЧЗёЪєгкНКЬхЃЌ
Д№АИЮЊЃКЖЁДяЖћаЇгІЃЛ
ЂкРћгУАыЭИФЄНјааЩјЮіПЩвдЬсДПНКЬхЃЌНКЬхЮЂСЃВЛФмЭИЙ§АыЭИФЄЃЌШмвКСЃзгПЩвдЭИЙ§АыЭИФЄЃЌЙЪФмДгАыЭИФЄРяЮіГіЕФЗжЩЂжЪТШЛЏФЦЃЌИУВйзїЕФУћГЦЪЧЩјЮіЃЛ
Д№АИЮЊЃК![]() ЃЛЩјЮіЃЛ
ЃЛЩјЮіЃЛ
ЃЈ4ЃЉЂйНКгШыКЃПкШ§НЧжоЕФаЮГЩЪЧгЩгкКгЫЎжаЕФНКЬхЮЂСЃОлГСдьГЩЕФЃЛ
ЙЪД№АИЮЊЃКОлГСЃЛ
ЂкЭСШРНКЬхНКСЃДјИКЕчЃЌЖд![]() ОпгаЮќИНзїгУЃЌПЩвдМѕЛКЦфСїЪЇЃЌЙЪЯѕЫсяЇЯѕЫсИљСїЪЇБШНЯЖрЃЛ
ОпгаЮќИНзїгУЃЌПЩвдМѕЛКЦфСїЪЇЃЌЙЪЯѕЫсяЇЯѕЫсИљСїЪЇБШНЯЖрЃЛ
Д№АИЮЊЃКЭСШРНКЬхНКСЃДјИКЕчЃЌЖд![]() ОпгаЮќИНзїгУЃЌПЩвдМѕЛКЦфСїЪЇЃЛ
ОпгаЮќИНзїгУЃЌПЩвдМѕЛКЦфСїЪЇЃЛ
Ђл![]() НКЬхжаЕФНКСЃЪЧаэЖрИі
НКЬхжаЕФНКСЃЪЧаэЖрИі![]() ЗжзгЕФОлМЏЬхЃЌЙЪ0.1 mol
ЗжзгЕФОлМЏЬхЃЌЙЪ0.1 mol![]() аЮГЩЕФНКСЃЪ§ФПаЁгк0.1 NAЃЛ
аЮГЩЕФНКСЃЪ§ФПаЁгк0.1 NAЃЛ
Д№АИЮЊЃКгЩгкНКСЃЪЧаэЖрИі![]() ЗжзгЕФОлМЏЬхЃЌЫљвдКЌга0.1 mol
ЗжзгЕФОлМЏЬхЃЌЫљвдКЌга0.1 mol ![]() ЕФБЅКЭШмвКжЦШЁ
ЕФБЅКЭШмвКжЦШЁ![]() ЪБЃЌаЮГЩЕФНКСЃЪ§ФПаЁгк0.1 NAЁЃ
ЪБЃЌаЮГЩЕФНКСЃЪ§ФПаЁгк0.1 NAЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЩњЛюГЃМћгУЦЗжаЃЌгаЙиЮяжЪЕФаджЪУшЪіВЛе§ШЗЕФЪЧЃЈ ЃЉ
бЁЯю | ЩњЛюгУЦЗ | УћГЦ | жївЊГЩЗж | аджЪ |
A |
| PPЫмСЯжЦзїЕФФЬЦП | ОлБћЯЉ | ФмЙЛЪЙЫсадИпУЬЫсМиЭЪЩЋ |
B |
| ЗЪдэ | ИпМЖжЌЗОЫсФЦ | ЗЪдэЕФЫЎШмвКГЪМюад |
C |
| ЗфУл | ЦЯЬбЬЧЁЂЙћЬЧКЭесЬЧ | есЬЧдкЯЁСђЫсЕФзїгУЯТПЩЫЎНтЩњГЩЦЯЬбЬЧКЭЙћЬЧ |
D |
| АЂНК | ТПЕФЦЄШЅУЋКѓАОжЦЖјГЩЕФНКПщ | дкКЯЪЪЕФУИЕФзїгУЯТФмЙЛЗЂЩњЫЎНтЗДгІ |
A.AB.BC.CD.D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвгУБъзМбЮЫсШмвКВтЖЈФГNaOHШмвКЕФХЈЖШЃЌгУМзЛљГШзїжИЪОМСЃЌЯТСаВйзїжаПЩФмЪЙВтЖЈНсЙћЦЋЕЭЕФЪЧЃЈ ЃЉ
A.ЫсЪНЕЮЖЈЙмдкзАЫсвКЧАЮДгУБъзМбЮЫсШмвКШѓЯД2ЁЋ3ДЮ
B.ПЊЪМЪЕбщЪБЫсЪНЕЮЖЈЙмМтзьВПЗжгаЦјХнЃЌдкЕЮЖЈЙ§ГЬжаЦјХнЯћЪЇ
C.зЖаЮЦПФкШмвКбеЩЋБфЛЏгЩЛЦЩЋБфГШЩЋЃЌСЂМДМЧЯТЕЮЖЈЙмвКУцЫљдкПЬЖШ
D.ЪЂNaOHШмвКЕФзЖаЮЦПЕЮЖЈЧАгУNaOHШмвКШѓЯД2ЁЋ3ДЮ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПВПЗжШѕЫсЕФЕчРыЦНКтГЃЪ§ШчБэЃК
ШѕЫс | HCOOH | HClO | H2CO3 | H2SO3 |
ЕчРыЦНКт ГЃЪ§ЃЈ25ЁцЃЉ | KaЃН1.77ЁС10Ѓ4 | KaЃН4.0ЁС10Ѓ8 | Ka1ЃН4.3ЁС10Ѓ7 Ka2ЃН4.7ЁС10Ѓ11 | Ka1ЃН1.54ЁС10Ѓ2 Ka2ЃН1.02ЁС10Ѓ7 |
ЃЈ1ЃЉЪвЮТЯТЂй0.1molЁЄL-1HCOONaЃЛЂк0.1molЁЄL-1NaClOЃЛЂл0.1molЁЄL-1Na2CO3ЃЛЂм0.1molЁЄL-1NaHCO3ЫФжжШмвКЕФpHгЩДѓЕНаЁЕФЙиЯЕЮЊ________________ЁЃЃЈгУађКХЬюПеЃЉ
ЃЈ2ЃЉХЈЖШОљЮЊ0.1 molЁЄLЃ1ЕФNa2SO3КЭNa2CO3ЕФЛьКЯШмвКжаЃЌSO32-ЁЂCO32-ЁЂHSO3-ЁЂHCO3-ХЈЖШДгДѓЕНаЁЕФЫГађЮЊ________________ЁЃ
ЃЈ3ЃЉЯТСаРызгЗНГЬЪНе§ШЗЕФЪЧ___________ЃЈЬюзжФИЃЉЁЃ
A.2ClO-+H2O+CO2=2HClO+CO32- B.2HCOOH+CO32-=2HCOO-+H2O+CO2Ёќ
C.H2SO3+2HCOO-=2HCOOH+SO32- D.Cl2+H2O+2CO32-=2HCO3-+Cl-+ClO-
ЃЈ4ЃЉФГЮТЖШЃЈTЁцЃЉЯТЕФШмвКжаЃЌcЃЈH+ЃЉ=10-xmolЁЄL-1ЃЌcЃЈOH-=10-ymolЁЄL-1ЃЌxгыyЕФЙиЯЕШчЭМЫљЪОЁЃ
ЂйДЫЮТЖШЯТЃЌ0.01mol/LЕФNaOHШмвКжаЫЎЕчРыГіЕФOH-ХЈЖШЮЊ_______ЁЃ
ЂкдкДЫЮТЖШЯТЃЌ0.1molЁЄL-1ЕФNaHSO4ШмвКгы0.1molЁЄL-1ЕФBa(OH)2ШмвКАДЯТБэжаМзЁЂввЁЂБћЁЂЖЁВЛЭЌЗНЪНЛьКЯЃК
Мз | вв | Бћ | ЖЁ | |
0.1molЁЄL-1ЕФBaЃЈOHЃЉ2 | 10 | 10 | 10 | 10 |
0.1molЁЄL-1ЕФNaHSO4 | 5 | 10 | 15 | 20 |
АДМзЗНЪНЛьКЯКѓЃЌЫљЕУШмвКЕФpHЮЊ____________ЃЛ
АДввЗНЪНЛьКЯКѓЃЌЦфЗДгІЕФРызгЗНГЬЪНЃК_________________ЁЃ
АДЖЁЗНЪНЛьКЯКѓЃЌЫљЕУШмвКЯд____________ЃЈЬюЁАЫсЁБЁАМюЁБЛђЁАжаЁБЃЉад
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПюыЭЪЧСІбЇЁЂЛЏбЇзлКЯадФмСМКУЕФКЯН№ЃЌЙуЗКгІгУгкжЦдьИпМЖЕЏаддЊМўЁЃвдЯТЪЧДгФГЗЯОЩяЇЭдЊМўЃЈКЌBeO25%ЁЂCuS71%ЁЂЩйСПFeSКЭSiO2ЃЉжаЛиЪеюыКЭЭСНжжН№ЪєЕФСїГЬЁЃ
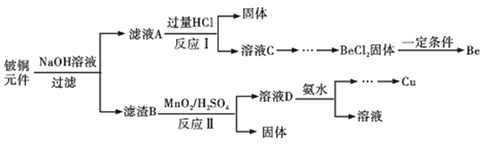
вбжЊЃК
ЂёЃЎюыЁЂТСдЊЫиДІгкжмЦкБэжаЕФЖдНЧЯпЮЛжУЃЌЛЏбЇаджЪЯрЫЦ
ЂђЃЎГЃЮТЯТЃКKsp[CuЃЈOHЃЉ2]=2.2ЁС10-20ЃЌKsp[FeЃЈOHЃЉ3]=4.0ЁС10-38ЃЌKsp[MnЃЈOHЃЉ2]=2.1ЁС10-13
(1)ТЫдќBЕФжївЊГЩЗжЮЊ______ЃЈЬюЛЏбЇЪНЃЉЃЛ
(2)аДГіЗДгІЂёжаКЌюыЛЏКЯЮягыЙ§СПбЮЫсЗДгІЕФЛЏбЇЗНГЬЪН______ЃЛ
(3)MnO2ФмНЋН№ЪєСђЛЏЮяжаЕФСђдЊЫибѕЛЏЮЊЕЅжЪСђЃЌаДГіЗДгІЂђжаCuSЗЂЩњЗДгІЕФРызгЗНГЬЪН______ЃЌШєгУХЈHNO3ШмНтН№ЪєСђЛЏЮяШБЕуЪЧ______ЃЈШЮаДвЛЬѕЃЉЃЛ
(4)ДгBeCl2ШмвКжаЕУЕНBeCl2ЙЬЬхЕФВйзїЪЧ______ЁЃ
(5)ШмвКDжаКЌcЃЈCu2+ЃЉ=2.2molL-1ЁЂcЃЈFe3+ЃЉ=0.008molL-1ЁЂcЃЈMn2+ЃЉ=0.01molL-1ЃЌж№ЕЮМгШыЯЁАБЫЎЕїНкpHПЩвРДЮЗжРыЪзЯШГСЕэЕФЪЧ______ЃЈЬюРызгЗћКХЃЉЃЌЮЊЪЙЭРызгПЊЪМГСЕэЃЌГЃЮТЯТгІЕїНкШмвКЕФpHДѓгк______ЃЛ
(6)ШЁюыЭдЊМў1000gЃЌзюжеЛёЕУBeЕФжЪСПЮЊ72gЃЌдђBeЕФВњТЪЪЧ______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІжаЃЌЫЎжЛзїбѕЛЏМСЕФЪЧ
ЂйЗњЦјЭЈШыЫЎжа ЁЁ ЂкЫЎеєЦјОЙ§зЦШШЕФНЙЬП ЁЁ ЂлФЦПщЭЖШыЫЎжа ЁЁ
ЂмЬњгыЫЎеєЦјЗДгІ ЁЁ ЂнТШЦјЭЈШыЫЎжа
A. жЛгаЂйЂм B. жЛгаЂйЂн
C. жЛгаЂкЂл D. жЛгаЂкЂлЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊ(Ђё)ЁЂ(Ђђ)ЗДгІдквЛЖЈЬѕМўЯТьЪБфМАЦНКтГЃЪ§ШчЯТЃК
2H2(g)ЃЋS2(g)2H2S(g) ІЄH1ЁЁK1ЁЁ(Ђё)
3H2(g)ЃЋSO2(g)2H2O(g)ЃЋH2S(g)ЁЁІЄH2ЁЁK2ЁЁ(Ђђ)
(1)гУІЄH1ЁЂІЄH2БэЪОЗДгІ4H2(g)ЃЋ2SO2(g)=S2(g)ЃЋ4H2O(g)ЕФІЄHЃН________ЁЃ
(2)ЛиД№ЯТСаЗДгІ(Ђё)ЕФЯрЙиЮЪЬтЃК
ЂйЮТЖШЮЊT1ЃЌдк1 LКуШнШнЦїжаМгШы1.8 mol H2ЁЂ1.2 mol S2,10 minЪБЗДгІДяЕНЦНКтЁЃВтЕУ10 minФкv(H2S)ЃН0.08 molЁЄLЃ1ЁЄminЃ1ЃЌдђИУЬѕМўЯТЕФЦНКтГЃЪ§ЮЊ________ЁЃ
ЂкЮТЖШЮЊT2ЪБ(T2ЃОT1)ЃЌдк1 LКуШнШнЦїжавВМгШы1.8 mol H2ЁЂ1.2 mol S2ЃЌНЈСЂЦНКтЪБВтЕУS2ЕФзЊЛЏТЪЮЊ25%ЃЌОнДЫХаЖЯІЄH1________0(ЬюЁАЃОЁБЛђЁАЃМЁБ)ЃЌгыT1ЪБЯрБШЃЌЦНКтГЃЪ§K1__(ЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
(3)ГЃЮТЯТЃЌгУSO2гыNaOHШмвКЗДгІПЩЕУЕНNaHSO3ЁЂNa2SO3ЕШЁЃ
ЂйвбжЊNa2SO3ЫЎШмвКЯдМюадЃЌдвђЪЧ________________(аДГіжївЊЗДгІЕФРызгЗНГЬЪН)ЃЌИУШмвКжаЃЌc(NaЃЋ)______2c(SO32-)ЃЋc(HSO3-)(ЬюЁАЃОЁБЁАЃМЁБЛђЁАЃНЁБ)ЁЃ
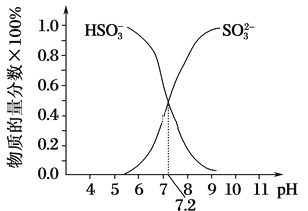
ЂкдкФГNaHSO3ЁЂNa2SO3ЛьКЯШмвКжаHSO3-ЁЂSO32-ЮяжЪЕФСПЗжЪ§ЫцpHБфЛЏЧњЯпШчЭМЫљЪО(ВПЗж)ЃЌИљОнЭМЪОЃЌдђSO32-ЕФЫЎНтЦНКтГЃЪ§ЃН________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАБЪЧжЦдьЛЏЗЪЕФживЊдСЯЃЌШчЭМЮЊЙЄвЕКЯГЩАБЕФСїГЬЭМЁЃЯТСагаЙиЫЕЗЈДэЮѓЕФЪЧ
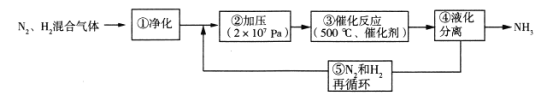
A.ЙЄвЕЩЯжЦЕЊЦјвЛАугУЗжРывКЬЌПеЦјЗЈ
B.ВНжшЂкЁЂЂлЁЂЂмЁЂЂнОљгаРћгкЬсИпЗДгІЮяЕФЦНКтзЊЛЏТЪ
C.ВНжшЂйжаЁАОЛЛЏЁБN2ЁЂH2ЛьКЯЦјЬхПЩвдЗРжЙДпЛЏМСжаЖО
D.ВНжшЂлжаЮТЖШбЁдё500ЁцЃЌжївЊЪЧПМТЧДпЛЏМСЕФЛюад
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкЯТЭМЕуЕЮАхЩЯНјааЫФИіШмвКМфЗДгІЕФаЁЪЕбщЃЌЦфЖдгІЗДгІЕФРызгЗНГЬЪНЪщаДе§ШЗЕФЪЧ(ЁЁЁЁ)

A. aЗДгІЃКFe2ЃЋЃЋ2HЃЋЃЋH2O2=Fe3ЃЋЃЋ2H2O
B. bЗДгІЃКHCO3-ЃЋOHЃ=CO32-ЃЋH2O
C. cЗДгІЃКHЃЋЃЋOHЃ=H2O
D. dЗДгІЃКAl3ЃЋЃЋ3NH3ЁЄH2O=Al(OH)3Ё§ЃЋ3NH4+
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com